
【题目】厨房垃圾发酵液可通过电渗析法处理,同时得到乳酸的原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )
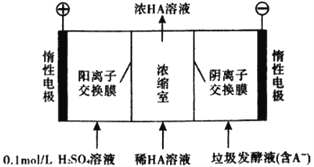
A. 通电后,阳极附近pH增大
B. 电子从负极经电解质溶液回到正极
C. 通电后,A—通过阴离子交换膜从阴极进入浓缩室
D. 当电路中通过2 mol电子的电量时,会有1 mol的O2生成
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】在不同条件下,分别测得反应2SO2+O2![]() 2SO3的化学反应速率,其中表示该反应进行最快的是( )
2SO3的化学反应速率,其中表示该反应进行最快的是( )
A. v(SO2)=4 mol·L-1·min-1 B. v(O2)= 3 mol·L-1·min-1
C. v(SO2)=0.1 mol·L-1·s-1 D. v(O2)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是一种重要的金属资源,在各领域都具有重要的作用。
(1)皮江法炼镁是我国生产镁的重要方法,其实质是在高温和真空条件下,有氧化钙存在时,通过硅还原氧化镁生成镁蒸气,与反应生成的固体硅酸二钙(2CaO·SiO2)相互分离,并经冷凝得到结晶镁。写出该反应的化学反应方程式 。
电解槽中先得到的是镁的蒸气,镁蒸气可以在下列 (填编号)气体氛围中冷却。
A.空气 B.氮气 C.水蒸气 D.氢气
(2)目前发达国家80%的镁来自于电解熔融氯化镁。电解原料无水氯化镁可由海水制备。主要有以下步骤:①在干燥的HCl气流中加热脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩冷却结晶。
其步骤先后顺序是_____________________(步骤可重复使用);在干燥的HCl气流中加热时,能得到无水MgCl2,其原因是______________________。
(3)已知某温度下Mg(OH)2的Ksp=6.4×l012,当溶液中c(Mg2+)≤1.0×105mol·L1可视为沉淀完全,则此温度下应保持溶液中c(OH-)≥_______________mol·L1。
(4)在Mg(OH)2悬浊液中滴入饱和NH4Cl溶液,溶液变澄清。反应原因可能有两个:一是NH4+水解产生H+,H+再与Mg(OH)2反应;二是_____________________(用离子方程式表示)。要验证谁是Mg(OH)2溶解的主要原因,可选取________代替NH4Cl溶液作对照实验。
A.NH4NO3 B.(NH4)2SO4 C.CH3COONH4 D.NH4HCO3
(5)镁电池是近年来科学技术研究的热点之一,下图为Mg—NaClO燃料电池结构示意图。其工作时Mg作 (填“X”或“Y”)电极,正极的电极反应式: 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途有对应关系的是
A. Al2O3熔点高,可用作耐高温材料 B. NH4HCO3受热易分解,可用作氮肥
C. Fe2(SO4)3易溶于水,可用作净水剂 D. SO2具有氧化性,可用于漂白纸浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某分子的球棍模型如下图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是( )
![]()
A. X原子可能为第ⅤA族元素
B. Y原子一定为第ⅠA族元素
C. 该分子中既含有极性共价键又含有非极性共价键
D. 从圆球的大小分析,该分子可能为N2F4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产中具有重要作用。
完成下列填空:

(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是____________;氮原子最外层电子有________种不同的能量,有_______种不同运动状态。
(2)NH3可以作制冷剂,是因为________________NH4Cl溶液与NaOH溶液混合至中性,则c(Na+)_______c(NH3H2O)(填“<,>”或“=”)
(3)写出一个能比较氮、氧两种元素非金属性强弱的事实:________________
研究NO2、SO2、CO等大气污染物的处理具有重要意义。NO2可用下列反应来处理:
![]()
(4)写出上述反应的平衡常数表达式_______________增大该反应平衡常数的措施有__________(填编号)
A. 增压 B. 增加NH3的浓度 C. 降温 D. 及时移走产物
(5)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是__________。(填编号)
A. c(NO2) : c(NH3)=3:4 B. ![]()
![]()
C. 容器内气体总压强不再变化 D. 容器内气体密度不再变化
(6)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测试NO2减少了0.75mol,则在2分钟内NH3的平均反应速率为: ![]() =_____________
=_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4P(红磷s)![]() P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
A. 正反应是一个放热反应
B. 当lmol白磷完全转变成红磷时放出17kJ热量
C. 当4g红磷转变成白磷时吸收17kJ热量
D. 白磷比红磷稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com