
【题目】重铬酸钾是工业合成的常用氧化剂和催化剂,如图所示的微生物电池,能利用K2Cr2O7实现对含苯酚(或醛类)废水的有效处理,该电池工作一段时间后,中间室内的NaC1溶液浓度减小,则下列叙述正确的是

A.a电极为负极,电子从a电极经过中间室到达b电极
B.M为阳离子交换膜,电解过程中中间室内的n(NaC1)减小
C.处理含苯甲醛废水时a电极反应式为:C6H5CHO-32e-+13H2O=7CO2+32H+
D.当b电极消耗等物质的量的K2Cr2O7时,a电极消耗的C6H5OH或C6H5CHO的物质的量之比为8:7
【答案】CD
【解析】
A.根据电池装置图可知,a极上苯酚或苯甲醛反应生成CO2,碳元素化合价升高发生氧化反应,故a极为负极,电子从a电极经过导线到达b电极,A错误;
B.因阴离子向负极移动,阳离子向正极移动,为保证电解质溶液导电的稳定性,M应为阴离子交换膜,中间室内的n(NaC1)减小,B错误;
C.处理含苯甲醛废水时,苯甲醛中碳元素失电子化合价升高生成CO2,根据元素和电荷守恒,电极反应式为C6H5CHO-32e-+13H2O=7CO2+32H+,C正确;
D. b极上,Cr2O72-中铬元素化合价降低生成Cr(OH)3,每消耗1mol K2Cr2O7转移6mol电子,当转移6mol电子时,根据电极反应式C6H5OH-28e-+11H2O=6CO2+28H+、C6H5CHO-32e-+13H2O=7CO2+32H+可知,消耗的的C6H5OH或C6H5CHO的物质的量之比为![]() ,D正确;
,D正确;
答案选CD。


科目:高中化学 来源: 题型:
【题目】有一无色溶液,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:

第③个实验中,生成白色沉淀的量与加入![]() 的量有如下图所示的相互关系。据此可知:
的量有如下图所示的相互关系。据此可知:

(1)在原溶液中一定存在的离子有______;一定不存在的离子有______;不能确定是否存在的离子有______。
(2)写出第③个实验中发生反应的离子方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是
A.![]() 的名称为2—羟基丁醇
的名称为2—羟基丁醇
B.![]() 的名称为2,3—二甲基—4—丙基—3—己烯
的名称为2,3—二甲基—4—丙基—3—己烯
C.![]() 与溴发生1:1加成反应,得到的有机产物有4种
与溴发生1:1加成反应,得到的有机产物有4种
D.分子式为C15H11Br,且不能发生消去反应的有机物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧杂环化合物R具有消炎、抗肿瘤的作用,分子结构如图所示,下列有关R的叙述错误的是
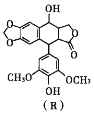
A.分子式为C21H22O8
B.分子中含有3种官能团
C.1mol R与NaOH溶液反应,最多消耗2mol NaOH
D.发生消去反应后的有机物分子中含有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是优良的多功能、绿色水处理剂。制备高铁酸钾的装置如图:
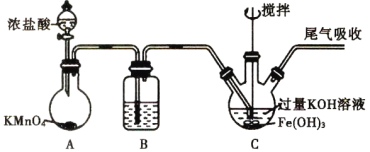
资料:①K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中比较稳定。②制备K2FeO4的反应为放热反应。下列叙述正确的是
A.装置A中的KMnO4可以用MnO2代替
B.装置B中的试剂为饱和碳酸氢钠溶液,目的是除去C12中的HC1
C.装置C中生成K2FeO4的关键操作是要缓慢通入Cl2且不能过量
D.K2FeO4做水处理剂时能杀菌消毒、吸附悬浮物与Cl2作用相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为气相直接水合法C2H4(g)+H2O(g)![]() C2H5OH(g)中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
C2H5OH(g)中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
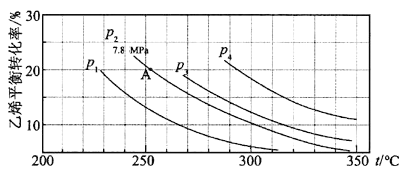
计算乙烯水合制乙醇反应在图中A点的平衡常数Kp为 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
A.0.082B.0.072C.0.072MPa-1D.0.082 MPa-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验与图象对应的是
选项 | A | B | C | D |
实验 | NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
图象 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行请根据上面流程,回答以下问题:
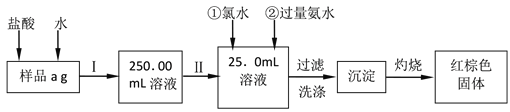
(1)操作I是配制溶液,所用到的玻璃仪器除烧杯、玻璃棒外,还必须有、_________。(填仪器名称)
(2)下列操作可能使所配溶液浓度偏小的是__________(填写序号)。
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入过量氨水时发生的离子反应方程式____________,
(4)检验沉淀是否已经洗涤干净的操作是__________。
(5)若原样品质量a为10g,加热后红棕色固体质量是6g,则样品中铁元素的质量分数是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)CH3OCH3(g)+H2O(g)△H=+23.5kJmol-1。在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。请回答下列问题:
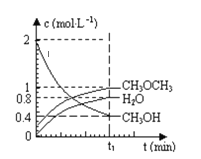
(1)该条件下反应平衡常数表达式K=___。在t1℃时,反应的平衡常数为___。用CH3OH表示的化学反应速率___。
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4molL-1、c(H2O)=0.6molL-1、c(CH3OCH3)=1.2molL-1,此时正、逆反应速率的大小:v(正)_____v(逆)(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com