
����Ŀ��һ�������£���һ���������ܱ������г���2molSO2��1molO2���������з�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)�ﵽƽ���ı�����������SO3(g)ƽ��Ũ�Ȳ��ı����
2SO3(g)�ﵽƽ���ı�����������SO3(g)ƽ��Ũ�Ȳ��ı����
A. �����¶Ⱥ�����������䣬����1mol SO3(g)
B. �����¶Ⱥ�������ѹǿ���䣬����1molO2(g)
C. �����¶Ⱥ�������ѹǿ���䣬����1mol SO3(g)
D. �����¶Ⱥ�������ѹǿ���䣬����1mol Ar(g)
���𰸡�C
��������A. ���º��ݣ�����1mol SO3(g)��ƽ��ʱ�൱����ԭ��1/2�����г�1molSO2��0.5molO2���������ݻ�һ����ƽ���淽���ƶ���SO3(g)ƽ��Ũ�ȸı䣬A����B. �����¶Ⱥ�������ѹǿ���䣬����1molO2(g)��ƽ�������ƶ���SO3(g)ƽ��Ũ�ȸı䣬B����C. ���º�ѹ������1mol SO3(g)��ƽ��ʱ�൱�ڳ�1molSO2��0.5molO2��ƽ�ⲻ�ƶ���SO3(g)ƽ��Ũ�Ȳ��ı䣬C��ȷ��D. ���º�ѹ������1mol Ar(g)���ݻ�����Ũ��С��ƽ�ⷢ���ƶ��ƶ���SO3(g)ƽ��Ũ�ȸı䣬D����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӹ��۵���������ұ�������ij��÷���������ԭ���������ȷ�Ӧ�������������ȷ�Ӧ��������������ұ����������(����)
A. ����þ B. ������ C. �������� D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Ļ���������ϡ����,�μ����軯����Һû����ɫ�仯,�ټ�����ˮ���ʺ�ɫ���� �� ��
A.FeSB.Fe2O3C.FeCl3D.Fe2(SO4)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ο�ʹ���ж���������ʳ�ؽ�����ʱ�����Ժ�___________�ⶾ��ԭ��������ʳƷ�к��н϶��_______________�����Ը��ؽ������γɲ�����ˮ�Ļ�������Լ����ؽ��������θ���Ĥ��Σ�������ⶾ�Ե����á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��ͬ�����£����и���Ӧ��Ϊ���ȷ�Ӧ�����С�Hֵ��С����
A��2A(g) +B(g) ==2C(l) ��H1
B��2A (g) +B(g) ==2C(g) ��H2
C��2A (l)+B(l)==2C(g) ��H3
D��2A (l) + B(l)==2C(l) ��H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽�����ܴﵽʵ��Ŀ�ĵ���
A. �÷�Һ©������ˮ���Ҵ�
B. ����ɫ��Ӧ����Na2SO4��K2CO3
C. �����۳�ȥFeCl2��Һ�к��е�����FeCl3
D. ��NaOH��Һ����ʵ��β���к��е�Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t��ʱ����2mol����A��1mol����B�����ݻ�Ϊ2L�ĺ����ܱ������У��������·�Ӧ��2A��g��+B��g��xC��g����2minʱ��ѧ��Ӧ�ﵽ�ȣ��¶���Ϊt�棩����ʱB���� 0.6mol�������C��Ũ��Ϊ0.6molL��1 �� ��ش��������⣺
��1���жϸ÷�Ӧ�ﵽ�ȵı�־�� a�������е�ѹǿ���ֲ���
b��A������������B����������֮��Ϊ2��1
c�������ڻ��������ܶȱ��ֲ���
d��A�İٷֺ������ֲ���
e��B��C�����ʵ���Ũ��֮��Ϊ1��x
��2��x= �� �ӷ�Ӧ��ʼ���ﵽ��ʱ����B��ʾ�÷�Ӧ��ƽ����Ӧ����V��B��=��
��3���������¶Ȳ��䣬�������������������Ӧ���������������С�����䡱��
��4����ѧ��Ӧ�ﵽ��ʱ��A��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������Ƭ���ܺ���Mg��Al��Cu�Ƚ������ʣ�ȡ��������Ƭ5.6 g��������ϡ���ᷴӦ���õ�0.2 g H2�������Ƭ��
A. һ���������� B. һ����������
C. һ��������ͭ D. һ���������ֽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ������֤Ԫ�������ɣ� �ù��������ˮ��Һ�Ͷ��������Ʊ�������������ͨ�뵽�����ᣨH2S��ˮ��Һ���У�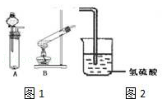
��1����������ĵ���ʽ����
��2����ͼ1��ѡ���������Ʊ�װ�� �� ��Ӧǰ��Ҫ�IJ����ǣ���
��3����ʵ�����֤��O�ķǽ�����ǿ��S���û�ѧ����ʽ��ʾ����
��4������Ϊ��֤��Cl�ķǽ�����ǿ��S���� a��S�ڳ�����Ϊ�����Cl2Ϊ���� b��H2S����HCl�ȶ�
c��H2SO3����������HClO3 d��S��H2���ϲ���Cl2��H2���Ͼ��ң�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com