
| A. | a>b>c | B. | a>c>b | C. | c>a>b | D. | c>b>a |
科目:高中化学 来源: 题型:选择题
| A. | 铝粉与MnO2高温条件下反应 | B. | 碳不完全燃烧产生CO | ||
| C. | 氢氧化钡晶体与氯化铵固体混合 | D. | 盐酸与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
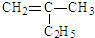
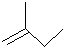
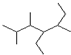 的名称2,3,5-三甲基-4-乙基庚烷
的名称2,3,5-三甲基-4-乙基庚烷 ②氢氧根离子
②氢氧根离子
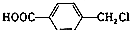 水解制得,写出K在浓硫酸作用下生成的聚合物的结构简式
水解制得,写出K在浓硫酸作用下生成的聚合物的结构简式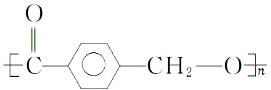 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
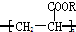 ,下列有关它的说法中,不正确的是( )
,下列有关它的说法中,不正确的是( )| A. | 它可由CH2=CH-COOR经加成聚合反应得到 | |
| B. | 在一定条件下能发生加成反应 | |
| C. | 聚丙烯酸酯材料是一种混合物 | |
| D. | 聚丙烯酸酯是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L苯的分子数约为NA个 | |
| B. | 常温下,在1moLC5H12中含有共价键数15NA | |
| C. | 标准状况下,17g NH3所含共价键数为NA个 | |
| D. | 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有② | B. | 只有②④ | C. | 只有②③④ | D. | 只有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
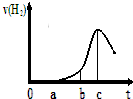 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.
某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
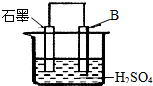 现有A、B、C三种短周期元素,原子序数依次递增.A与C的质子数之和为27,最外层电子数之差为5;0.9g单质B与足量盐酸反应,收集到气体1.12L(标准状况).请回答下列问题:
现有A、B、C三种短周期元素,原子序数依次递增.A与C的质子数之和为27,最外层电子数之差为5;0.9g单质B与足量盐酸反应,收集到气体1.12L(标准状况).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2CO3固体溶于1L水中配成溶液,其物质的量浓度为1mol/L | |
| B. | 40g NaOH固体溶于100g水,配成的溶液质量百分比浓度为40% | |
| C. | 22.4L氨气溶于水配成1L溶液,其物质的量浓度为1mol/L | |
| D. | 1mol NaCl固体溶于水配成1L溶液,其物质的量浓度为1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com