
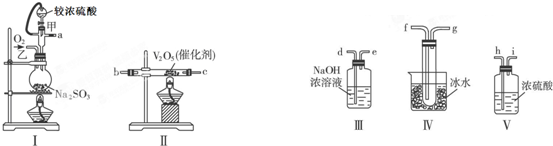
| 二氧化硫的减少量 |
| 二氧化硫的初始量 |
| 64n-m |
| 64n |
| 64n-m |
| 64n |


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N60是N2的同素异形体 |
| B、N60的稳定性比N2差,熔沸点比N2低 |
| C、N60是原子晶体 |
| D、N60可能会成为很好的火箭材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
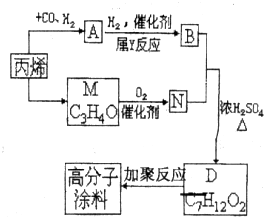 有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.查看答案和解析>>
科目:高中化学 来源: 题型:
| 试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ① | 取少量该焰火原料加入冷水 | 无明显现象 | 不含有Li、Na等活泼金属 |
| ② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体 |
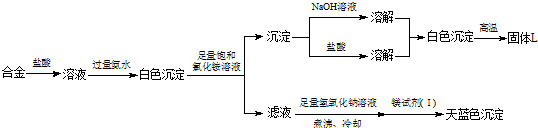
 问题讨论:
问题讨论: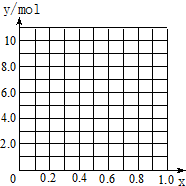
查看答案和解析>>
科目:高中化学 来源: 题型:
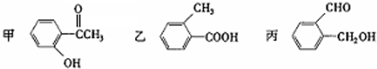
查看答案和解析>>
科目:高中化学 来源: 题型:
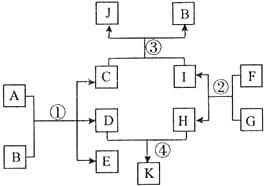 在如图所示的物质转化关系中(反应条件已略去).A是海水中含量最多的盐,B是最常见的无色液体,D、E、F、H为单质.反应①是海水资源综合利用的重要反应,反应②常用于钢轨的焊接,工业上用C与D反应制备漂白液.
在如图所示的物质转化关系中(反应条件已略去).A是海水中含量最多的盐,B是最常见的无色液体,D、E、F、H为单质.反应①是海水资源综合利用的重要反应,反应②常用于钢轨的焊接,工业上用C与D反应制备漂白液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com