
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
将0.1 mol·L-1的下列物质的水溶液,从常温加热到90 ℃,溶液的pH几乎不变的是(不考虑水的蒸发)( )
A.氯化钠 B.氢氧化钾 C.硫酸 D.硫酸铵
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
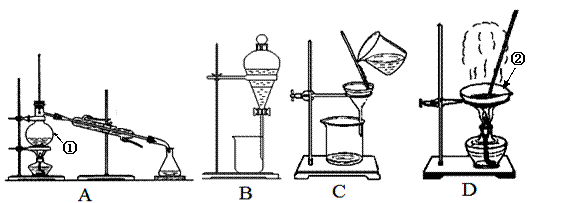
(1)装置A中仪器①的名称是 ,装置D中仪器②的名称是 。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置 (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置 ;从碘水中分离出I2,选择装置 ,该装置的主要仪器名称是 。
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用 的方法除去
Fe(OH)3胶体中混有的杂质Cl-离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应
B.XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强
C.非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强
D.Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关系中,A是一种正盐,D的分子量比C的分子量大16,E是酸;当X无论是强碱还是强酸时都有如下转化关系:
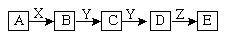
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强酸时,A、B、C、D、E均同时含有另一种元素。回答下列问题:(用化学式填写)
(1)A是_____________,Y是______________,Z是____________。
(2)当X是强碱时,写出B与Y反应的化学方程式:___________________________。
(3)当X是强酸时,写出C与Y反应的化学方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案设计中,可行的是 ( )
A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B.用萃取的方法分离汽油和煤油
C.用溶解、过滤的方法分离KNO3和NaCl固体的混合物
D.将H2和O2的混合气体通过灼热的氧化铜,以除去其中的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
实验题(14分):
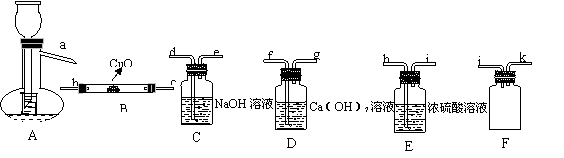 Ⅰ、HCOOH是一种无色、易挥发的液体,某学习小组参照:
Ⅰ、HCOOH是一种无色、易挥发的液体,某学习小组参照: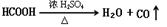 原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
(1)若所制气体流向从左向右时,上述仪器连接为:
A→( ) →( )→( )→( ) →( )
(2)A装置中小试管的作用(至少答两条):
① 。② 。
(3)证明HCOOH受热产物中有CO的现象为: 。
(4)本实验有3处用到酒精灯,除A、B处外,还缺一个酒精灯,应放在 处.
Ⅱ、学习小组查阅资料知:
①Cu的颜色为红色或紫红色,而Cu2O的颜色也为红色或砖红色。
 |
②4CuO 2 Cu2O + O2↑ ③ Cu2O +2H+=Cu + Cu2+ + H2O 因此对CO充分还原CuO后所得红色固体是否含有Cu2O进行了认真的研究,提出下列设计方案:
方案①:取该红色固体溶于足量稀硝酸中,观察溶液颜色的变化。
方案②:取该红色固体溶于足量稀硫酸中,观察溶液颜色的变化。
(5)写出Cu2O与稀硝酸反应的化学方程式: 。
(6)请你评价方案②的合理性,并简述理由:
方案②: ,理由: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下面两个小题:
Ⅰ.(11分)月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1) 3He是高效核能原料,其原子核内中子数为___________。
(2)Na的原子结构示意图为_______,Na在氧气中完全燃烧所得产物的电子式为______。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点__________(填“高”或”低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,SiO2的晶体类型为_________;所含化学键类型为 。
③MgO与碳粉和足量氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐有___________________ (写化学式)。
Ⅱ.(13分)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d 轨道中有9个电子。
请回答下列问题:
(1)Y基态原子的电子排布式是________________;Z所在周期中第一电离能最大的主族元素是_________。
 (2) XY2- 离子的立体构型是_____________:R2+的水合离子中,提供孤电子对的原子是________。
(2) XY2- 离子的立体构型是_____________:R2+的水合离子中,提供孤电子对的原子是________。
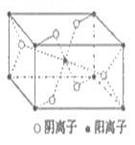
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数比是__________。
(4)将R的硫酸盐溶液中通入足量氨气,充分反应后溶液呈
深蓝色,该反应的离子方程式是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com