
| A、F |
| B、Mg2+ |
| C、Cl- |
| D、Ca2+ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2[CaCO3] |
| B、Fe(OH)3[Fe2O3] |
| C、KI[I2] |
| D、NaOH[Na2CO3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
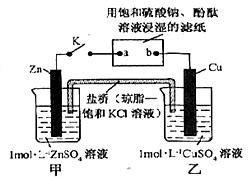
| A、电子沿Zn→a→b→Cu路径流动 |
| B、铜电极上发生氧化反应 |
| C、盐桥中的K+向甲烧杯移动 |
| D、片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、硫离子的结构示意图: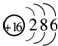 | ||
B、NH4Cl的电子式: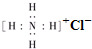 | ||
C、原子核内有10个中子的氧原子:
| ||
| D、水的结构式:H-O-H |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在炽热碎瓷片的作用下,石蜡油分解产生了可以使酸性高锰酸钾溶液褪色的乙烯 |
| B、葡萄糖遇碘水会变蓝,油脂是产生能量最高的营养物质 |
| C、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| D、甲苯能与溴水反生化学反应,乙醇不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Li在氧气中燃烧主要生成Li2O2 | ||||
| B、实验室制备Cl2可用排饱和食盐水集气法收集 | ||||
C、
| ||||
| D、碱金属和卤素的单质的熔沸点随原子序数递增均依次升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com