
| A、冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 |
| B、“血液透析”利用了胶体的性质 |
| C、“PM2.5”是细小颗粒物悬浮在空气中形成胶体,严重危害人体健康 |
| D、电解质在水溶液和熔融状态下均能导电 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
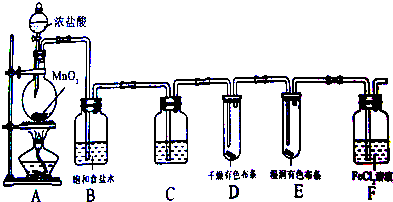
查看答案和解析>>
科目:高中化学 来源: 题型:
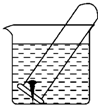 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
如图所示,水槽中试管内有一枚铁钉,放置数天观察:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化硼液态时能导电而固态时不导电 |
| B、氯化硼加到水中使溶液的pH升高 |
| C、氯化硼分子呈平面正三角形,属非极性分子 |
| D、氯化硼B-Cl之间是sp3形成的σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、424 | B、212 |
| C、116.6 | D、106 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知Ra是第七周期、ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强 |
| B、已知As是第四周期、ⅤA族的元素,故AsH3的稳定性比NH3的稳定性强 |
| C、已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈 |
| D、已知Cl的核电荷数比Al的核电荷数大,故Cl的原子半径比Al的原子半径小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池的正极、电解池的阴极都有电子流入 |
| B、原电池的正极、电解池的阳极都发生氧化反应 |
| C、原电池的负极质量一定减少 |
| D、电解池的阳极不参加反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com