
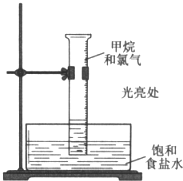
 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )| 现象 | 解释 | |
| A. | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B. | 量筒内出现少量白雾 | 生成HCl气体 |
| C. | 量筒内壁产生油状液滴 | 油状液体是CCl4 |
| D. | 量筒中液面降低 | 生成液态产物 |
| A. | A | B. | B | C. | C | D. | D |
分析 甲烷在光照条件下与氯气发生取代反应,生成产物中一氯甲烷为气体,二氯甲烷、三氯甲烷和四氯化碳为液态,反应中还有氯化氢生成,以此解答该题.
解答 解:A.量筒内气体颜色逐渐变浅,是由于氯气与甲烷发生取代反应,甲烷中C化合价升高,被氧化,故A错误;
B.发生取代反应生成氯化氢,氯化氢易溶于水,产生白雾,故B正确;
C.甲烷与氯气发生取代反应生成二氯甲烷、三氯甲烷和四氯化碳为液态,所以油状液滴可能为二氯甲烷、三氯甲烷和四氯化碳等,故C错误;
D.量筒中液面降低是由于生成氯化氢易溶于水导致,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重甲烷的取代反应等知识,题目难度中等,充分考查学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
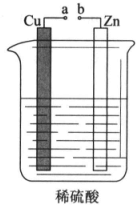 课外小组的同学对如图所示的实验装置进行了研究.
课外小组的同学对如图所示的实验装置进行了研究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
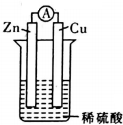 在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是( )
在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是( )| A. | 锌片是正极,铜片上有气泡产生 | |
| B. | 电流方向是从锌片流向铜片 | |
| C. | 溶液中的阳离子向正极移动,阴离子向负极移动 | |
| D. | 经过一段时问工作后'电解液的pH值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
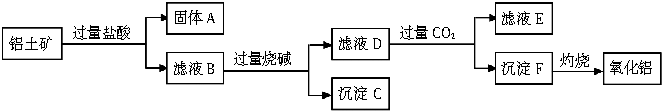
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
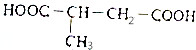
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com