
(13��)��ͼ��Ԫ�����ڱ���һ���֣����еĢ١�����Ԫ�أ��û�ѧ������ջش�
�� ���� | I A | IIA | IIIA | ��A | VA | ��A | ��A | 0 |
�� |
|
|
| �� | �� |
| �� |
|
�� |
| �� | �� | �� |
|
| �� | �� |
�� | �� |
|
|
|
|
| �� |
|
��1������ЩԪ���У���ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ ��
��2��д���ٵ����������͢ڵĵ��ʵĵ���ʽ �� ��
��3���õ���ʽ��ʾ������γɻ�����Ĺ��� ��
��4���ٵĵ��ʺ͢������ﷴӦ�Ļ�ѧ����ʽ ��
��5��д���ݵĵ������������Ʒ�Ӧ�Ļ�ѧ����ʽ��
д���ݵ���������������������Һ��Ӧ�����ӷ���ʽ�� ��
��6����֪��l mol C��H����l mol O=O����l molC=O����l mol H��O���ֱ���Ҫ���յ�����Ϊ414kJ��498kJ��728kJ��464kJ����l mol������ȫȼ�շų� kJ��������
��1��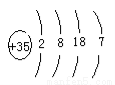
��2��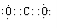
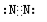
��3��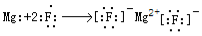
��4��2C+SiO2 Si+2CO��;
Si+2CO��;
��5��2Al+2H2O +NaOH=2NaAlO2+3H2��;Al(OH)3+OH-=AlO-2+2H2O��
��6��660
��������
�����������1����ԭ����Brԭ�ӣ�������35�����ӣ�ԭ�ӽṹʾ��ͼΪ ��
��
��2���ٵ������������CO2������ʽΪ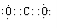 ���ڵĵ�����N2������ʽΪ
���ڵĵ�����N2������ʽΪ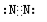 ��
��
��3��������γɻ�������MgF2���������ӻ����Mgʧȥ2�����ӳ�Ϊþ���ӣ�F�õ�1�����ӳ�Ϊ�����ӣ��õ���ʽ��ʾ���γɹ�����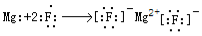 ��
��
��4���ٵĵ��ʺ͢������ﷴӦ��C�������������·����û���Ӧ����ѧ����ʽΪ2C+SiO2 Si+2CO��;
Si+2CO��;
��5������Al�����������Ʒ�Ӧ�Ļ�ѧ����ʽΪ2Al+2H2O +NaOH=2NaAlO2+3H2��;�����������������д���ӷ���ʽʱ���ܲ�������������������������Һ��Ӧ�����ӷ���ʽΪAl(OH)3+OH-=AlO-2+2H2O��
��6������������ȼ�յĻ�ѧ����ʽΪCH4+2O2 CO2+ 2H2O�����ݷ�Ӧ���뻯ѧ�����ܵĹ�ϵ����H=��4��414+2��498-2��728-2��2��464��kJ/mol=-660 kJ/mol������1mol������ȫȼ�շų�660kJ��������
CO2+ 2H2O�����ݷ�Ӧ���뻯ѧ�����ܵĹ�ϵ����H=��4��414+2��498-2��728-2��2��464��kJ/mol=-660 kJ/mol������1mol������ȫȼ�շų�660kJ��������
���㣺����Ԫ�����ڱ���Ӧ�ã�Ԫ�ص�����Ӧ�ã���ѧ����ı�ʾ����ѧ��ЧӦ�ļ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�걱���з�̨��������ѧ��ͳһ��ϰ��һ����ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪A(g)+B(g)  C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830��ʱ����һ��2 L���ܱ������г���0.2mol��A��0.8mol��B����Ӧ��ʼ4 s��A��ƽ����Ӧ����v(A)=0��005 mol/(L��s)������˵����ȷ����
A��4 sʱc(B)Ϊ0.76 mol/L
B��830���ƽ��ʱ��A��ת����Ϊ80%
C����Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D��1200��ʱ��ӦC(g)+D(g) A(g)+B(g)��ƽ�ⳣ����ֵΪ0.4
A(g)+B(g)��ƽ�ⳣ����ֵΪ0.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���Ϻ�����㡢�ɽ�����ɽ����������ģ��ѧ�Ծ��������棩 ���ͣ������
�����仯�����������������д��ڹ㷺��;�����������ա�
��1����ͼ��ʾΪ��Ԫ�������ڱ��е���Ϣ�������С�55.85��������Ϊ�� ����ԭ�Ӻ����� ���˶�״̬��ͬ�ĵ��ӡ�

��2����ï��[Fe(C5H5)2]��һ���л�����������۵�172�棬�е�249�棬��������������ˮ�������л��ܼ�����ï������ ���壻�ⶨ������ï����������ԭ�ӵĻ�ѧ��������ͬ�����ï���ĽṹӦΪͼ�е� ��ѡ�a����b������
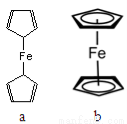
��3���̷���FeSO4��7H2O������������ȱ����ƶѪ����ˮ��Һ¶���ڿ����л���ʣ�
д���������ʷ�Ӧ�����ӷ���ʽ ��
��4����ˮFeCl3��ˮ������������ʪ���������������������տ����е�ˮ�ֳ�Ϊ�ᾧ�Ȼ���(FeCl3��6H2O)���Ʊ���ˮFeCl3���Լ��� ��
��5����������Ҳ�dz��õ�ˮ���������������ƣ�Na2FeO4���������·�Ӧ�Ʊ���
2FeSO4 + 6Na2O2 �� 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2����������2mol Na2FeO4����Ӧ�е���ת�Ƶ����ʵ���Ϊ mol��
��6���������οɽ�ˮ���е�Mn2+����ΪMnO2���г�ȥ���������� Mn2+ 1mg��ˮ����������Ҫ1.2 mg/L������� L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���Ϻ�����㡢�ɽ�����ɽ����������ģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������Ĵ�������˵������ܳ��ֽ����Ե���
A��IBr B��I2O5 C��I3+ D��I3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(6��)��ij���������ȴ���Ӧ�����һ�ȴ���ֻ��1�֡�7.2 g������ȫ����һ�ȴ���ʱ���ų�������������ˮ��ȫ���գ�������Һ��0.2 mol��L-1NaOH��Һ500 mLǡ���к͡���������ķ���ʽΪ ����ṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�״��ڴ����������ṩ����(H+)�͵��ӣ����Ӿ����·�����Ӿ��ڵ�·������һ����������Ӧ������ܷ�ӦʽΪ2CH3OH+3O2 2CO2+4H2O�����й��ڸõ�صķ������ټ״��Ǹ�����H+���ƶ��۸�����Ӧ��CH3OH-6e-+H2O=CO2+6H+ ��1 mol CH3OH��ȫ��Ӧת��12 mol���� ��������Ӧ��O2+4e-+2H2O==4OH- �õ�صĵ������Һ�����Ǽ�Һ��������ȷ����
2CO2+4H2O�����й��ڸõ�صķ������ټ״��Ǹ�����H+���ƶ��۸�����Ӧ��CH3OH-6e-+H2O=CO2+6H+ ��1 mol CH3OH��ȫ��Ӧת��12 mol���� ��������Ӧ��O2+4e-+2H2O==4OH- �õ�صĵ������Һ�����Ǽ�Һ��������ȷ����
A���٢ڢ� B���ڢۢܢ� C���� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ṹ�У������ڵ�˫������ṹ��������Ϊ֤�ݵ���ʵ��
�ٱ�����ʹKMnO4(H+)��Һ��ɫ���ڱ�������̼ԭ�ӵľ������ȣ��۱�����һ�������¸�H2�ӳ����ɻ����飻�ܾ�ʵ�����ڶ��ױ���һ�ֽṹ���ݱ���FeBr3����������ͬҺ�巢��ȡ����Ӧ��������ѧ�仯��ʹ��ˮ��ɫ��
A���ڢۢܢ�B���٢ۢܢ�C���٢ڢܢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����к����������ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪NA���������ӵ�����������˵����ȷ����
A����״���£�22��4 L O2��O3��ɵĻ������ԭ������Ϊ2NA
B��1 mol���������������ϡ���ᷴӦʱ��ת�Ƶ�������3NA
C���ں�Al3+����ΪNA��AlCl3��Һ�У�Cl-����Ϊ3NA
D��1 mol�ؼ�(-CD3)���е�����Ϊ9NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����кӶ���������ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��ij���ӵĵ�����������������������ӿ�����һ�ַ��ӻ�һ������
B�����ɵ��ʵķ�����һ�����й��ۼ�
C����Һ�ͽ���ı����������������ЧӦ
D.��ѧ�仯��������Ԫ�أ�������Ԫ�صı仯���ǻ�ѧ�仯
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com