
| A. | 服用铬含量超标的药用胶囊会对人体健康造成危害 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 | |
| D. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 |
分析 A.药用胶囊超标的铬,是重金属盐,能使蛋白质发生变性;
B.血液为胶体,“血液透析”运用了胶体的性质;
C.明矾溶于水发生水解反应,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质;
D.新型复合材料具有强度大、刚度好、重量轻等特点特点,可以制造出具有较好性价比的特殊结构的产品.
解答 解:A.铬是重金属,能使蛋白质发生变性,服用铬含量超标的药用胶囊会对人体健康造成危害,故A正确;
B.利用血液透析进行治疗因肾功能衰竭等疾病引起的血液中毒,是利用来了血液是胶体,不会通过半透膜的原理,故B正确;
C.明矾[KAl(SO4)2•12H2O]作为净水剂是因为明矾溶于水发生水解反应,反应的离子方程式为:Al3++3H2O?Al(OH)3+3H+,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质,能做净水剂,但不能作漂白剂,故C错误;
D.新型复合材料具有强度大、刚度好、重量轻等特点特点,所以新型复合材料使手机、电脑等电子产品更轻巧,实用和新潮,故D正确.
故选C.
点评 本题考查了生活中常见物质的性质及用途,注意知识的迁移和应用在解题中的应用是解题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、液氨(电解质) | |
| B. | CO2(非电解质)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质) | |
| C. | HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃) | |
| D. | NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
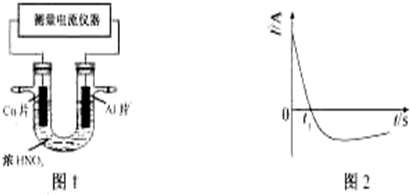
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L | B. | 5.6L | C. | 4.48L | D. | 2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2和H2SO4;Cu(OH)2和CH3COOH | B. | Ba(OH)2和Na2SO4;Ba(OH)2和CuSO4 | ||
| C. | NaOH和H2SO4;NaOH和NaHSO4 | D. | Na2CO3和盐酸;NaHCO3和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 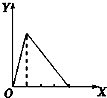 向NaOH溶液中逐滴加入AlCl3溶液至过量且边滴边振荡 | |
| B. | 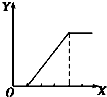 向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡 | |
| C. | 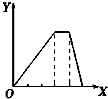 向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量 | |
| D. | 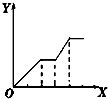 向NaOH、Ba(OH)2、NaA1O2的混合溶液中逐渐通入二氧化碳至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2分子比H原子更稳定 | |
| B. | 可求出Cl-Cl 的键能为428 kJ/mol | |
| C. | 1mol氢气与1mol氯气所含的总能量比2mol HCl所含的总能量高 | |
| D. | 理论上利用此反应制取盐酸的同时,可依据原电池原理获取电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com