
| 充电 |
| 放电 |
| A、放电时,电子从b极通过电解质流向a极 |
| B、放电时,每转移0.2mol电子,消耗2.4g的Mg |
| C、电解质是含镁离子的水溶液 |
| D、充电时,b极上的电极反应式为:Mg2++FeSO4+2E=MgFeSO4 |
| 充电 |
| 放电 |
| 充电 |
| 放电 |


科目:高中化学 来源: 题型:
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性大于Y的电负性 |
| C、X的氧化性小于Y的氧化性 |
| D、X的第一电离能小于Y的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是SO2与O2在接触室中多段催化氧化2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)回答下列问题:
如图是SO2与O2在接触室中多段催化氧化2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 20.00 | 24.01 |
| 2 | 20.00 | 23.99 |
| 3 | 20.00 | 22.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol?L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
| ② | 反应物浓度越大,反应速率越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
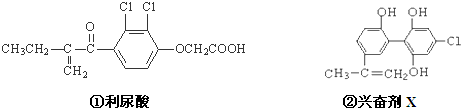
| A、利尿酸乙酯分子中有三种含氧官能团,在核磁共振氢谱上共有七个峰 |
| B、1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2 |
| C、两种兴奋剂最多都能和含3molNaOH的溶液反应 |
| D、两种分子中的所有碳原子均不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大压强,化学反应速率一定增大 |
| B、化学反应速率为反应时间内反应物浓度的增加或者生成物浓度的减少 |
| C、升高温度,化学反应速率一定增大 |
| D、加入反应物,化学反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在氯乙烷中直接加入AgNO3溶液 |
| B、在氯乙烷中加蒸馏水,然后加入AgNO3溶液 |
| C、在氯乙烷中加入NaOH溶液,加热,冷却后酸化,然后加入AgNO3溶液 |
| D、在氯乙烷中加入乙醇,加热,冷却后酸化,然后加入AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com