

 +Br2
+Br2| FeBr3 |
 +HBr,
+HBr, +Br2
+Br2| FeBr3 |
 +HBr;
+HBr;

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、钢筋混凝土、玻璃钢、石棉瓦、碳纤维增强陶瓷都是常见的复合材料 |
| B、蛋白质、棉花、核酸、PVC、淀粉、油脂都是由高分子组成的物质 |
| C、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| D、煤经气化和液化两个物理过程后可变为清洁能源,这是煤综合利用的主要方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧原子发生SP杂化 |
| B、该分子为V型分子 |
| C、氧原子与H、Cl都形成π键 |
| D、该原子的电子式为H:O:Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
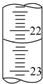 实验室中有一未知浓度的稀盐酸,某学生用0.10mol?L-1 NaOH标准溶液进行测定盐酸的浓度的实验.取20.00mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生用0.10mol?L-1 NaOH标准溶液进行测定盐酸的浓度的实验.取20.00mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.请完成下列填空:| 实验编号 | 待测盐酸的体积(mL) | NaOH溶液的浓度(mol?L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2SO3?2SO2+O2 |
| B、H2PO4-+H2O?HPO42-+H3O+ |
| C、Fe3++3H2O?Fe(OH)3+3H+ |
| D、CH3COOH+OH-?CH3COO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
试验编号 | T/K | V水/ml | V(Na2S2O3)/ml | V(H2SO4)/ml | 实验目的 |
| ① | 298 | 10 | 5 | 5 | 实验①和②探究温度对该反应速率的影响. 实验①和③探究 对化学反应速率的影响. 实验①和④探究 对化学反应速率的影响. |
| ② | 308 | 10 | 5 | 5 | |
③ | 298 | Vx | 10 | 5 | |
| ④ | 298 | 10 | 5 | 5 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体于试管中,加适量蒸馏水溶解 | |
| 步骤2:向试管中加入 | |
| 步骤3:取 | 若有白色沉淀生成,证明固体中混有Na2SO4;若无白色沉淀生成,证明固体中无Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
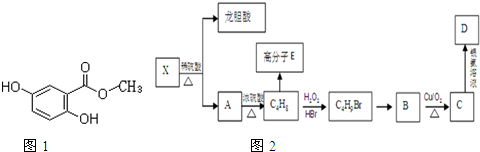
| H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、NO3-、MnO4- |
| B、Mg2+、Na+、Cl-、SO42- |
| C、K+、Na+、Br-、Cu2+ |
| D、Na+、Ba2+、OH-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com