
| A. | 丙烷的二卤代物是4种,则其六卤代物是2种 | |
| B. | 对二甲苯的核磁共振氢谱显示有3种化学环境的氢 | |
| C. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种 | |
| D. | 某烃的同分异构体只能形成一种一氯代物,其分子式可能为C5H12 |
分析 A、采用换元法,将氯原子代替氢原子,氢原子代替氯原子,从二氯代物有四种同分异构体,就可得到六氯代物也有四种同分异构体;
B、对二甲苯属于对称结构,其中含有2种化学环境的氢;
C、甲苯苯环上有3种H原子,含3个碳原子的烷基取代有正丙基、异丙基,据此计算判断;
D、先判断烷烃的同分异构体,再确定烷烃的对称中心,即找出等效的氢原子,据此解答即可.
解答 解:A、丙烷有8个H原子,其中2个H原子被氯原子取代形成丙烷的二氯代物.六氯代物可以看作C3Cl8中的8个氯原子,其中2个氯原子被2个氢原子代替形成,两者是等效的.氯代物有四种同分异构体,可得到六氯代物也有四种同分异构体,故A错误;
B、对二甲苯属于对称结构,其中含有2种化学环境的氢,即苯环上一种,甲基上一种,故B错误;
C、甲苯苯环上有3种H原子,含3个碳原子的烷基有正丙基、异丙基两种,所以甲苯苯环上的一个氢原子被含3个碳原子的烷基取代有3×2=6产物,故C错误;
D、C5H12戊烷有正戊烷、异戊烷、新戊烷3种同分异构体,正戊烷CH3CH2CH2CH2CH3有3种氢原子,所以一氯代物有3种;异戊烷CH3CH(CH3)CH2CH3有4种氢原子,所以一氯代物有4种;新戊烷CH3C(CH3)2CH3有1种氢原子,所以一氯代物有1种,符合题意,故D正确,故选D.
点评 本题考查了同分异构体的判断,难度较大,先确定烃的同分异构体,再确定等效氢原子,最后根据氢原子的种类确定一氯代物的种类,会确定等效氢原子是解本题的关键.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:多选题
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、CH3COOH均为共价化合物 | |
| B. | 每生成1molCH3COOH,要消耗22.4LCO2 | |
| C. | CO2、CH3COOH分子中均含σ键和π键 | |
| D. | CH4$→_{-H_{2}}^{催化剂}$CHX属于氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
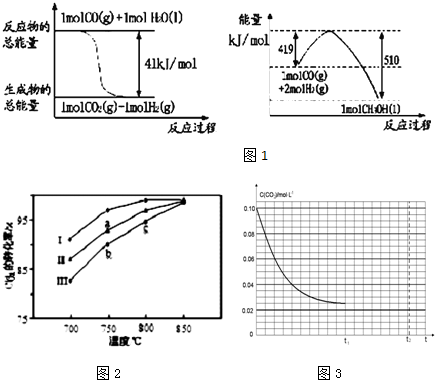
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时0.1mol/LX2W溶液的pH>1-lg2 | |
| B. | 溶液中水的电离程度:RYX>R2W | |
| C. | 热稳定性:X2Y>X2W | |
| D. | 由X、Y、Z、W、R五种元素组成的一种化合物可作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
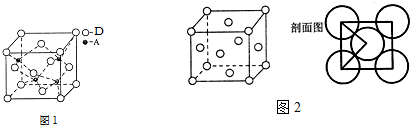
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
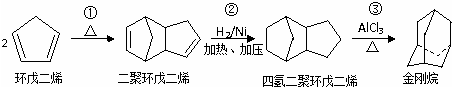
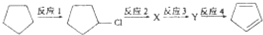
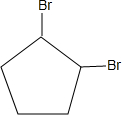 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$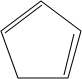 +2NaBr+2H2O;
+2NaBr+2H2O;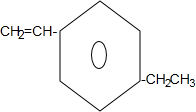 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 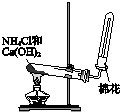 用a制备并收集氨气 | B. | 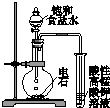 用b制备并检验乙炔 | ||
| C. | 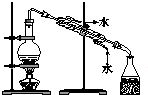 用c蒸馏海水得到淡水 | D. | 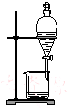 用d分离Na2CO3溶液与CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{11.2X}{5A}$mol-1 | B. | $\frac{5A}{11.2X}$mol-1 | C. | $\frac{22.4A}{5X}$mol-1 | D. | $\frac{22.4X}{5A}$mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com