
| A、溶液碱性:KOH>LiOH |
| B、溶液酸性:HNO3<H2CO3 |
| C、原子半径:S<F |
| D、硫与氢气反应比氟与氢气反应更容易 |


科目:高中化学 来源: 题型:
| A、在燃煤中添加石灰石粉末以减少酸雨的发生 |
| B、为实现“低碳世博”,上海世博会很多展馆采用光电转化装置 |
| C、对所有垃圾通过露天焚烧或深埋的方式进行处理 |
| D、利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn>Cu>Ag |
| B、Zn>Ag>Cu |
| C、Cu>Ag>Zn |
| D、Ag>Cu>Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应过程中无沉淀产生 |
| B、参加反应的HCl共0.4mol |
| C、金属在反应中共失去0.4mol电子 |
| D、钠镁共0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
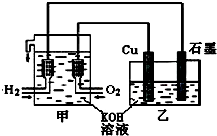 利用如图装置制取Cu2O,乙的总反应化学方程式为:2Cu+H2O=Cu2O+H2↑.下列说法正确的是( )
利用如图装置制取Cu2O,乙的总反应化学方程式为:2Cu+H2O=Cu2O+H2↑.下列说法正确的是( )| A、乙中Cu电极的电极反应式是:2Cu+2OH--2e-=Cu2O+H2O |
| B、甲中通入氧气的电极为负极 |
| C、乙中阴离子向石墨电极移动 |
| D、电路上通过0.5mol电子,可制得0.5mol Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水显碱性:NH3?H2O═NH4++OH- |
| B、Na2S溶液显碱性:S2-+2H2O?H2S+2OH- |
| C、硫酸氢钠溶液显酸性:NaHSO4═Na++H++SO42- |
| D、AlCl3溶液显酸性:Al3++3H2O?Al(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01 mol?L-1的蔗糖溶液 |
| B、0.01 mol?L-1的CaCl2溶液 |
| C、0.01 mol?L-1的NaCl溶液 |
| D、0.02 mol?L-1的CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 汽车尾气是城市主要空气污染物,研究控制汽车尾气成为保护环境的重要任务.
汽车尾气是城市主要空气污染物,研究控制汽车尾气成为保护环境的重要任务.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com