
| A. | ①④ | B. | ②③ | C. | 只有① | D. | 只有④ |
分析 铊和铝都位于周期表第ⅢA族,原子核外有3个电子,最高化合价为+3价,能形成+3价的离子化合物,同主族元素从上到下元素的原子半径逐渐增大,对应金属单质的还原性逐渐增强,由此分析解答.
解答 解:①同主族元素从上到下原子半径逐渐增大,所以铊原子半径比Al大,故正确;
②同主族元素从上到下元素的金属性逐渐增强,则铊的金属性强于铝,所以Tl(OH)3不是两性氢氧化物,故错误;
③从上到下金属单质的还原性依次增强,所以Tl>Al,对应最高价阳离子的还原性就越弱,所以Tl3+的氧化性比Al3+弱,故错误;
④稀硝酸具有强氧化性,与金属反应生成NO和硝酸盐,故正确.
故选A.
点评 本题考查同主族元素的性质的递变规律,题目难度不大,本题注意把握相关性质的递变规律.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 中和时所需KOH 的量 | B. | CH3COOH电离程度 | ||
| C. | H+的物质的量浓度 | D. | CH3COOH的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
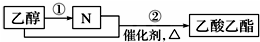
| A. | N为乙酸 | |
| B. | 可用饱和碳酸钠溶液除去乙酸乙酯中混有的N | |
| C. | 过程①中可加入LiAlH4等还原剂将乙醇转化为N | |
| D. | 过程②如果加热一段时间后发现忘记加碎瓷片,应停止反应,待冷却后补加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和O3互为同素异形体 | |
| B. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H互为同位素 | |
| C. | CH2═CH2和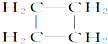 互为同系物 互为同系物 | |
| D. | 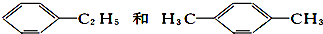 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
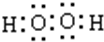 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24LCO2中含有的原子数为0.3NO | |
| B. | 1.8g NH4+离子中含有的质子数为NO | |
| C. | C60和石墨的混合物共1.8g,含碳原子数目为0.15NO | |
| D. | 在0.1mol/L K2CO3溶液中,阴离子数目大于0.1NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com