
| A. | CH2=CH2是还原剂,PbCl2是氧化剂 | B. | CuCl2是还原剂,O2是氧化剂 | ||
| C. | 乙烯是还原剂,O2是氧化剂 | D. | PbCl2和CuCl2都是氧化剂 |
分析 在氧化还原反应中,得电子化合价降低的物质作氧化剂,失电子化合价升高的物质作还原剂,据此分析解答.
解答 解:①CH2=CH2+PdCl2+H2O→CH3CHO+2HCl+Pd
②Pd+2CuCl2=PdCl2+2CuCl的反应中
③2CuCl+1/2O2+2HCl=2CuCl2+H2O
将方程式①+②+③得CH2=CH2+$\frac{1}{2}$O2=CH3CHO,该反应中氧气是氧化剂,乙烯是还原剂;
A.乙烯是还原剂,PdCl2是催化剂,故A错误;
B.氯化亚铜催化剂,氧气是氧化剂,故B错误;
C.乙烯是还原剂,氧气是氧化剂,故C正确;
D.PdCl2和CuCl都是催化剂,故D错误;
故选C.
点评 本题考查了氧化还原反应中还原剂、还原剂的判断,难度不大,明确元素的化合价是解本题的关键,注意PdCl2和CuCl都是催化剂,为易错点.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应产物的总焓与反应物的总焓之差,称为反应焓变 | |
| B. | 反应产物的总焓小于反应物的总焓,该反应为放热反应 | |
| C. | 同一反应在不同温度下进行,其焓变是相同的 | |
| D. | 已知2NO2(g)═N2O4(g)△H1,N2O4(g)═2NO2(g)△H2,则△H1=-△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
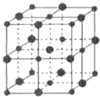 已知X、Y、Z、M、Q五种元素的原子序数依次递增;X、Y、M三种元素组成的一种化合物A是新装修居室中常含有的一种有害气体.Q4+离子和氩原子的核外电子排布相同.
已知X、Y、Z、M、Q五种元素的原子序数依次递增;X、Y、M三种元素组成的一种化合物A是新装修居室中常含有的一种有害气体.Q4+离子和氩原子的核外电子排布相同.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 在化合物Na2O2中,阴、阳离子的个数比为1:1 | |
| C. | 在化合物CaCl2中,两个氯离子之间存在共价键 | |
| D. | 含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体1可能为SO2和CO2的混合物 | |
| B. | 沉淀3可能为Al(OH)3 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com