
向一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2  5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
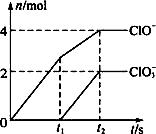
试回答:
(1)t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为_________ mol,该石灰乳中含有的Ca(OH)2的质量是_________ g。
(2)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入氯气的速率不同,n(ClO-)和n (ClO3-)的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后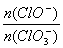 _____2(填“>”“<”或“=”)。
_____2(填“>”“<”或“=”)。
(3)若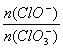 =a,则n(Cl-)=_________ mol(用含a的代数式表示)。
=a,则n(Cl-)=_________ mol(用含a的代数式表示)。
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,100g98%硫酸溶液中含有的氧原子数为4NA
B.标准状况下,当活泼金属转移2NA个电子时,可从盐酸中置换产生44.8LH2
C.15gCH3+中含有的电子数为0.8NA
D.1molH2O2分子中非极性共价键数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝
 (3)阳极氧化能使金属表面生成
(3)阳极氧化能使金属表面生成
致密的氧化膜。以稀硫酸为电解液,铝
阳极发生的电极反应式为
__________________________________。
(4)在铝阳极氧化过程中,需要不断
地调整电压,理由是____________ ___
。
(5)下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
下面关于Na2CO3和NaHCO3的叙述,不正确的是( )
A、在水中的溶解度:Na2CO3 >NaHCO3
B、热稳定性:Na2CO3 >NaHCO3
C、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者产生的CO2少
D、足量的Na2CO3和NaHCO3分别与等物质的量的 盐酸反应,两者产生的CO2一样多
盐酸反应,两者产生的CO2一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,在三个烧瓶内分别装有干燥、纯净的NH3、含一半空气的氯化氢气体、NO2和O2体积比为4∶1的混合气体。然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2∶1∶2 B.5∶5∶4
C.1∶1∶1 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应生成的有机产物一定是纯净物的是 ( )
A. 1,3-丁二烯与等物质的量的Br2发生反应
B. 2-氯丁烷与NaOH水溶液共热
C. 甲苯与浓硝酸在浓硫酸存在下发生反应生成一硝基甲苯
D. 氯乙烯在一定条件下反应生成聚氯乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:
CH2=CH2(g) + H2O(g)  CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是 ( )
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是 ( )
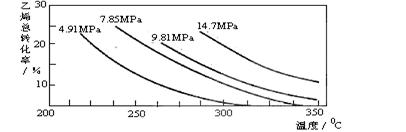
A.合成乙醇的反应一定为吸热反应
B.目前工业上采用250~300℃,主要是在此温度下乙烯的转化率最大
C.目前工业上采用加压条件(7MPa左右),目的是提高乙醇的产率和加快反应速率
D.相同催化剂下,在300℃ 14.7MPa乙醇产率反而比300℃ 7MPa低得多,是因为加压平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是
A.铜片加入三氯化铁溶液中:Cu+2Fe3+===== 2Fe2++Cu2+
B.盐酸中加入碳酸钙:CO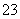 +2H+===== H2O+CO2↑
+2H+===== H2O+CO2↑
C.AlCl3溶液中加入足量的氨水:Al3++3OH-===== Al(OH)3↓
D.NaHCO3溶液中加入盐酸:CO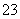 +2H+===== H2O+CO2↑
+2H+===== H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
化工厂的设计是将实验室的研究成果转化为工业化生产的重要的基础工作。
(1)以硫铁矿为原料生产硫酸需经过 、 和 三个主要生产阶段。
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
①索尔维制碱法的原理是 。(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 。
③侯氏制碱法可以循环使用的物质有 。
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。
电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com