
| A. | 硅胶可防止食物受潮是由于其具有吸水性 | |
| B. | 持续加热到一定温度能杀死甲型H1N1流感病毒是因为病毒蛋白质受热变性 | |
| C. | 纤维素在人体内可水解为葡萄糖是人类重要的营养物质之一 | |
| D. | 酸性重铬酸钾用于检查酒驾是利用其强氧化性 |
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:选择题
| A. | 用H2O2酸性溶液,将海带灰中的I-转变为I2:H2O2+2I-═I2+2OH- | |
| B. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 工业电解熔融氯化钠制金属钠:2Na++2Cl-$?_{熔融}^{电解}$2Na+Cl2↑ | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液洗气时发生反应的离子方程式为:2OH-+Cl2═Cl-+ClO-+H2O | |
| B. | 根据实验可以得出中性条件下,氧化性Cl2>O2 | |
| C. | 根据实验可以得出反应物的浓度和溶液的pH会影响物质的氧化性 | |
| D. | 根据实验现象可以判断电解时阳极的电极反应式为:2Cl--2e-═Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H11Br有7 种同分异构体 | |
| B. | 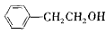 能发生取代、加成、氧化、消去等反应 能发生取代、加成、氧化、消去等反应 | |
| C. | 合成纤维和光导纤维都是新型无机非金属材料 | |
| D. | 溴丙烷水解制丙醇和丙烯与水反应制丙醇的反应类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
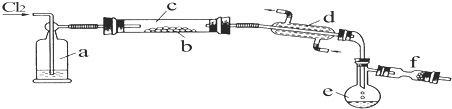
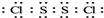 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②⑤ | C. | ①②④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com