
| A. | 直径为1.3×10-9m 的“钴酞菁”分子分散在水中能形成胶体,则该分子的直径比Na+大 | |
| B. | 煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体 | |
| C. | 丁达尔现象可以用来区别胶体和溶液 | |
| D. | 明矾净水利用了胶体的性质 |
分析 A.胶体分散系直径在1-100nm,溶液中分散质直径小于1nm;
B.向沸水中加饱和FeCl3溶液来制备Fe(OH)3胶体;
C.丁达尔效应是胶体所特有的性质;
D.明矾在溶液中电离出的铝离子能水解生成氢氧化铝胶体,氢氧化铝胶体能净水.
解答 解:A.“钴酞菁”分子(直径为1.3×10-9米)的微粒直径属于胶体分散系范围内,属于胶体分散系,溶液中分散质直径小于1nm,所以“钴酞菁”分子的直径比Na+大,故A正确;
B.向沸水中加饱和FeCl3溶液,当溶液呈红褐色时,停止加热,即可得到Fe(OH)3胶体,煮沸饱和FeCl3溶液容易得到Fe(OH)3沉淀,故B错误;
C.丁达尔效应是胶体所特有的性质,所以丁达尔现象可以用来区别胶体和溶液,故C正确;
D.明矾在溶液中电离出的铝离子能水解生成氢氧化铝胶体,氢氧化铝胶体能吸附水中的悬浮颗粒,所以能净水,故D正确.
故选B.
点评 本题考查了胶体的性质,注意把握胶体的性质以及胶体与其它分散系的本质区别,题目难度不大,侧重于基础知识的考查.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol?L-1 A1C13溶液中含有的Al3+数目小于NA | |
| B. | 标准状况下,11 g3H216O中含有的质子数目为6NA | |
| C. | 1 mol Li2O和Na2O2的混合物中含有的离子总数大于3NA | |
| D. | 常温常压下,4.6 g NO2所含的氮原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
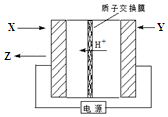 氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )| A. | 图中所示电极中,X端为负极,Y端为正极 | |
| B. | Y参与的电极反应为H2+2e-=2H+ | |
| C. | 反应过程中左边区域溶液pH逐渐升高 | |
| D. | 当有3gH+通过质子交换膜时,Z的体积为11.2L(标况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
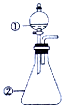 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠混合溶液 | 立即产生气泡 |
| B | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| C | 氯化铁溶液 | 淀粉碘化钾溶液 | 溶液变为蓝色 |
| D | 硫酸亚铁溶液 | 过氧化钠固体 | 产生气泡和白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 除去乙烷中混有的少量乙烯:将混合气体通入足量酸性KMnO4溶液中 | |
| C. | 提取溶解在水中的少量碘:加入CCl4振荡、静置、分层后放出下面有机层再分离 | |
| D. | 检验某溶液中是否含有甲醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
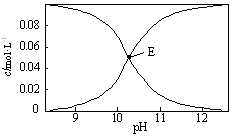 20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )
20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )| A. | pH=9的溶液中:c(HCO3-)>c(H2CO3)>c(CO32-) | |
| B. | c(HCO3-)=c(CO32-)的E点溶液中:c(OH-)+c(CO32-)>c(H+)+c(H2CO3)+0.050 mol•L-1 | |
| C. | pH=11的溶液中:c(Na+)<2c(CO32-)+c(HCO3-) | |
| D. | 0.100 mol•L-1的Na2CO3溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,则一定有:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) | |
| B. | 1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 物质的量浓度分别为c1和c2的两种醋酸溶液,若其pH分别为a和a+1,则c1>10c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| a.取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| b.取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| c.取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| d.取少量该溶液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于HNO3 |
| e.取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com