
| A、5.6g铁在足量氯气中燃烧,电子转移0.3NA个 |
| B、标准状况下,2.24L水中含有0.1NA个水分子 |
| C、1.12L氯气中反应0.1NA个氯原子 |
| D、12g石墨和C60的混合固体中,含碳原子NA个 |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
 已知:N2O4(g)?2NO2(g)△H=+57.20kJ?mol-1.
已知:N2O4(g)?2NO2(g)△H=+57.20kJ?mol-1.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol/L | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol/L | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(HCO3-)<c(CO32-) |
| B、c(HCO3-)>c(HSO3-) |
| C、c(CO32-)+c(HCO3-)═c(SO32-)+c(HSO3-) |
| D、两溶液都能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验时手掌不小心沾上苯酚,应立即用65℃以上的热水清洗防腐蚀 |
| B、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| C、实验室可以用浓硫酸与氯化钠固体共热制取氯化氢气体,因此浓硫酸与碘化钠固体共热也能制取碘化氢气体 |
| D、用化学方法检验甘油和酒精:可用新制的Cu(OH)2悬浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
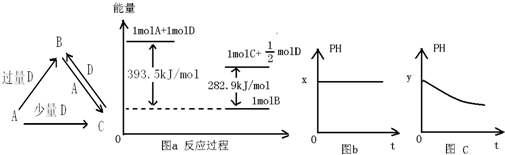
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
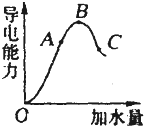 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图所示.请回答:
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图所示.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com