
| A. | 在此反应中硝酸体现强氧化性,全部被还原 | |
| B. | 向反应后的溶液中再加入金属铁,不再发生化学反应 | |
| C. | 该反应中被还原的硝酸与未被还原的硝酸之比为1:4 | |
| D. | 该反应中被还原的硝酸与未被还原的硝酸之比为1:5 |
分析 物质的量之比为1:3的锌与稀硝酸反应,设Zn的物质的量为1mol则硝酸的物质的量为3mol,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,锌完全溶解转移电子物质的量=1mol×(2-0)=2mol,根据转移电子相等生成n(N2O)=$\frac{2mol}{(5-1)×2}$=0.25mol,根据N原子守恒得作氧化剂硝酸的物质的量=2n(N2O)=2×0.25mol=0.5mol,起酸作用硝酸物质的量=2n[Zn(NO3)2]=2×1mol=2mol,所以消耗总的硝酸物质的量=0.5mol+2mol=2.5mol<3mol,则硝酸有剩余,据此分析解答.
解答 解:物质的量之比为1:3的锌与稀硝酸反应,设Zn的物质的量为1mol则硝酸的物质的量为3mol,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,锌完全溶解转移电子物质的量=1mol×(2-0)=2mol,根据转移电子相等生成n(N2O)=$\frac{2mol}{(5-1)×2}$=0.25mol,根据N原子守恒得作氧化剂硝酸的物质的量=2n(N2O)=2×0.25mol=0.5mol,起酸作用硝酸物质的量=2n[Zn(NO3)2]=2×1mol=2mol,所以消耗总的硝酸物质的量=0.5mol+2mol=2.5mol<3mol,则硝酸有剩余,
A.根据以上分析知,在此反应中硝酸体现强氧化性、酸性,部分被还原,故A错误;
B.硝酸有剩余,所以向反应后的溶液中再加入金属铁,会发生化学反应,故B错误;
C.被还原硝酸的物质的量是0.5mol,未被还原硝酸的物质的量=3mol-0.5mol=2.5mol,所以该反应中被还原的硝酸与未被还原的硝酸之比=0.5mol:2.5mol=1:5,故C错误;
D.根据C知,该反应中被还原的硝酸与未被还原的硝酸之比为1:5,故D正确;
故选D.
点评 本题以锌和稀硝酸的反应为载体考查氧化还原反应方程式的有关计算,正确判断溶液中的溶质是解本题关键,易错选项是CD,注意未被还原的硝酸还包含没有反应的硝酸,题目难度中等.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水、浓H2SO4 | B. | KMnO4(H+)、浓H2SO4 | ||
| C. | 溴水、NaOH溶液、浓H2SO4 | D. | 浓H2SO4、KMnO4(H+)、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
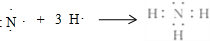 .写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
.写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
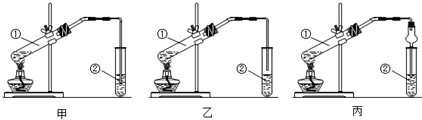
 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国发射的“嫦娥三号”卫星中使用的碳纤维,是一种新型无机非金属材料 | |
| B. | 只要符合限量,“食用色素”“碘元素”、“亚硝酸盐”可以作为某些食品的添加剂 | |
| C. | 氢氧化铁溶胶、水玻璃、淀粉溶液均具有丁达尔效应 | |
| D. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com