
����Ŀ��A��B��C��D��E��F��G��Ϊ�л������A ����������һ������ʯ�ͻ�����չˮƽ�ı�־�����ʣ�����֮��������ת����ϵ����֪ȩ�������������������Ȼ�����ش��������⣺ 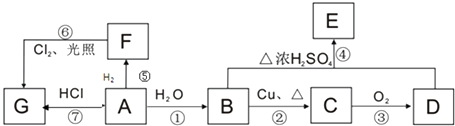
��1��A��B�й����ŵ����ƣ�A��B��
��2����F��ͬϵ��������л���Ŀռ乹��Ϊ��
��3��д����F��Ϊͬϵ��ĺ�5��̼ԭ�ӵ�����ͬ���칹����һ�ȴ����������ٵĽṹ��ʽ��
��4��д�����б�Ŷ�Ӧ��Ӧ�Ļ�ѧ��Ӧ����ʽ����ע����Ӧ���ͣ� ������Ӧ��
������Ӧ��
���𰸡�
��1��̼̼˫�����ǻ�
��2����������
��3��C��CH3��4
��4��2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��������CH3CH2OH+CH3COOH
2CH3CHO+2H2O��������CH3CH2OH+CH3COOH ![]() CH3CH2OOCCH3+H2O��������ȡ������Ӧ
CH3CH2OOCCH3+H2O��������ȡ������Ӧ
���������⣺A ����������һ������ʯ�ͻ�����չˮƽ�ı�־�����ʣ���AΪCH2=CH2����ϩ��ˮ�����ӳɷ�Ӧ����BΪCH3CH2OH���Ҵ���������������CΪCH3CHO����ȩ��һ������������Ӧ����DΪCH3COOH���������Ҵ�����������Ӧ����EΪCH3COOCH2CH3 �� ��ϩ�����������ӳɷ�Ӧ����FΪC2H6 �� ��ϩ��HCl��������GΪCH3CH2Cl����������������ȡ����Ӧ���������飮��1��AΪCH2=CH2 �� ���й�����Ϊ��̼̼˫����BΪCH3CH2OH�����й�����Ϊ���ǻ������Դ��ǣ�̼̼˫�����ǻ�����2��FΪC2H6 �� ��F��ͬϵ��������л���Ϊ���飬�ռ乹��Ϊ�������壬���Դ��ǣ��������壻��3��FΪC2H6 �� ��F��Ϊͬϵ��ĺ�5��̼ԭ�ӵ�����ͬ���칹��Ľṹ��ʽ��CH3CH2CH2CH2CH3 �� CH3CH2CH��CH3��2 �� C��CH3��4 �� ����һ�ȴ����������ٵ�ΪC��CH3��4 �� ���Դ��ǣ�C��CH3��4����4����Ӧ�����Ҵ�����������Ӧ������ȩ����Ӧ����ʽΪ2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O����Ӧ�����������Ҵ�����������Ӧ����������������Ӧ����ʽΪ�����Դ��ǣ�2CH3CH2OH+O2
2CH3CHO+2H2O����Ӧ�����������Ҵ�����������Ӧ����������������Ӧ����ʽΪ�����Դ��ǣ�2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��������Ӧ��CH3CH2OH+CH3COOH
2CH3CHO+2H2O��������Ӧ��CH3CH2OH+CH3COOH ![]() CH3CH2OOCCH3+H2O��������ȡ������Ӧ��
CH3CH2OOCCH3+H2O��������ȡ������Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E���ֶ���������Ԫ�أ�ԭ��������A��E������AԪ�������������Ǵ�����������2������B�������Ӻ�C������������ԭ�ӵĵ��Ӳ�ṹ��ͬ������ͨ��״���£�B�ĵ��������壬0.1mol B��������������������ȫ��Ӧ����0.4mol����ת�ƣ���C�ĵ����ڵ�ȼʱ��B�ĵ��ʳ�ַ�Ӧ�����ɵ���ɫ�Ĺ��壬�˵���ɫ��������AB2��Ӧ������B�ĵ��ʣ���D����̬�⻯��������ۺ�������ܷ���������ԭ��Ӧ����д����
��1��AԪ�ص����������Ľṹʽ��BԪ�������ڱ��е�λ�� ��
��2��C������B������ȼ�յ���������������ѧ����������C��D ���γɻ�����ĵ���ʽ ��
��3��DԪ�صĵͼ���������E�ĵ��ʵ�ˮ��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��4��Ԫ��D��Ԫ��E��ȣ��ǽ����Խ�ǿ��������Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ��������ѡ����ţ��� a��������D�ĵ��ʺ�E�ĵ���״̬��ͬ b��E���⻯���D���⻯���ȶ�
c��һ��������D��E�ĵ��ʶ������Ʒ�Ӧ d��D����ۺ�������������E����ۺ�����
e��D�ĵ�������E���⻯�ﷴӦ����E���ʣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ʵ�����ڼ�����������ȡCl2�Ļ�ѧ����ʽΪ��MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O���ֽ�8.7 g MnO2Ͷ�뵽200 g��������Ϊ36.5%(����)��Ũ�����м��ȣ���ַ�Ӧ����
MnCl2��Cl2����2H2O���ֽ�8.7 g MnO2Ͷ�뵽200 g��������Ϊ36.5%(����)��Ũ�����м��ȣ���ַ�Ӧ����
��1����״��������Cl2�������
��2����Ӧ���ɵ�MnCl2������Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ���� �� ��
A. ��״���£�18gH218O����������Ϊ10NA
B. 1molOH-�����еĵ�����Ϊ9NA
C. Na2O2��H2O�ķ�Ӧ�У�ÿ����0.1molO2��ת�Ƶ�����ĿΪ0.2NA
D. 1molMgCl2�к��е�������Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʽΪC3H6Cl2���л��������һ����ԭ�ӱ���ԭ��ȡ��������������ֿ��ܵĽṹ��ԭ�л���Ľṹ��ʽΪ��������
A.CH2Cl��CH2��CH2Cl
B.CHCl2��CH2��CH3
C.CH2Cl��CHCl��CH3
D.CH3��CCl2��CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʢ��NO��NO2 �Ļ���������Ͳ������ʢ��ˮ��ˮ���У���һ��ʱ�����Ͳ�ڵ����������СΪԭ����һ�룮
��1��д���йط�Ӧ�Ļ�ѧ����ʽ��
��2��ԭ���������NO��NO2��������Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F�����ڱ�ǰ�����ڵ�Ԫ�أ�ԭ������������A�Ļ�̬ԭ��2p�ܼ�����2����������C�ǵؿ��к�������Ԫ����E�ĵ��ʳ��³�ѹ��Ϊ����ɫ���壬��ѧ����ʮ�ֻ��ã����ж�����Fλ��ds���������ܲ��е����ӣ����Ⱥ͵���ѵ���֮һ��D��F��ͬ���ڣ��������ܲ��������ȡ�
��1��д����̬Cԭ�ӵĵ����Ų�ʽ: ____________��
��2��A��B��C����Ԫ�ص�һ������������____________��(��Ԫ�ط��ű�ʾ)����ԭ����____________��
��3��B��C��Ԫ���γɵĻ�����B2C�ķ��ӿռ乹��Ϊ____________����B2C��Ϊ�ȵ���������ӵĻ�ѧʽΪ____________��(��һ��)��
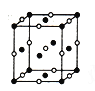
��4��D��E�γɵ�һ�����ӻ�����ھ����ṹͼ�к����ʾE��λ�ã������ʾD��λ�ã���֪�þ����ı߳�Ϊncm,�����ӵ�����ΪNA�������ܶ���=_______g/cm3(�ú�n��NA�ļ���ʽ��ʾ)��
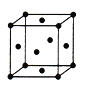
��5����Fԭ���γɵľ����ṹ��ͼ��Fԭ�ӵİ뾶Ϊr����ʽ��ʾFԭ���ھ����еĿռ�������:__________________(��Ҫ�������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��������X��Y�����ܱ������з�����Ӧ����Z��5min��ﵽƽ�⣮���ʼŨ�Ⱥ�ƽ��Ũ�����±���
���� | X | Y | Z |
��ʼŨ��/molL��1 | 0.1 | 0.2 | 0 |
ƽ��Ũ��/molL��1 | 0.05 | 0.05 | 0.1 |
����˵��������ǣ� ��
A.�÷�Ӧ�ɱ�ʾΪX+3Y2Z
B.��Ӧ�ﵽƽ��ʱ��X��ת����Ϊ50%
C.ǰ5min ��Y��ʾ��ƽ����Ӧ����Ϊ�ԣ�Y��=0.01 molL��1min��1
D.����ѹǿʹƽ��������Z�ķ����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com