
| A. | FeCl3溶液能用于腐蚀铜线路板 | B. | 用小苏打治疗胃酸过多 | ||
| C. | 过氧化钠作供氧剂 | D. | 用还原性铁粉作食品抗氧化剂 |
分析 发生的反应中含元素的化合价变化,则与氧化还原反应有关;反之,不存在元素的化合价变化,无氧化还原反应发生,以此来解答.
解答 解:A.Cu与氯化铁反应生成氯化铜、氯化亚铁,Cu、Fe元素的化合价变化,为氧化还原反应,故A不选;
B.小苏打与盐酸反应生成二氧化硫、水、氯化钠,无元素的化合价变化,无氧化还原反应发生,故B选;
C.过氧化钠作供氧剂,生成氧气,O元素的化合价变化,为氧化还原反应,故C不选;
D.用还原性铁粉作食品抗氧化剂,Fe元素的化合价变化,为氧化还原反应,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
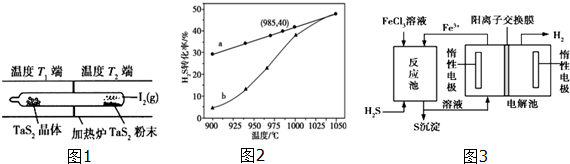
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
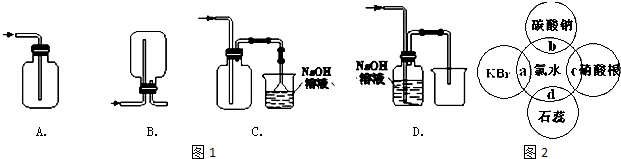
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
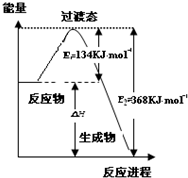 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| C. | 1mol烃基与17gNH3所含电子数之比为9:10 | |
| D. | 一定温度下1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl含NH4+的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 与铝反应产生氢气的溶液中:Na+、NH4+、SO42-、CH3C00- | |
| B. | c(Fe3+)=0.1mol•L-1的溶液中:NH4+、Cl-、AlO2-、SO42- | |
| C. | 使甲基橙变红的溶液中:K+、Al3+、SO42-、NO3- | |
| D. | 由水电离出的c(OH-)=10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
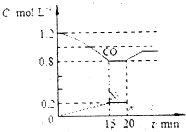 CO和NO对环境影响较大,属于当今社会热点问题.请回答下列问题
CO和NO对环境影响较大,属于当今社会热点问题.请回答下列问题| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com