
分析 (1)酸中c(H+)=10-pH mol•L-1=10-amol•L-1,碱中c(OH-)=10pH-14 mol•L-1=10b-14 mol•L-1=10-amol•L-1,可见酸中c(H+)与碱中c(OH-)相等,2Va=Vb混合后溶液的pH小于7,说明溶液呈酸性,应为弱酸与强碱的组合;
(2)酸中c(H+)=10-pH mol•L-1=10-amol•L-1,碱中c(OH-)=10pH-14 mol•L-1=10b-14 mol•L-1=10-(a+1)mol•L-1,据滴定过程中,氢离子浓度=$\frac{n({H}^{+})}{{V}_{混合液}}$计算.
(3)pH=a的强酸c(H+)=10-amol/L,pH=b的强碱c(OH-)=10b-14mol/L,恰好中和,则有Va×10-a=Vb×10b-14,结合Va<Vb,a=0.5b计算.
解答 解:(1)解:pH=a的酸的溶液中c(H+)=10-pH mol•L-1=10-amol•L-1,
a+b=14,则pH=b的碱中c(OH-)=10pH-14 mol•L-1=10b-14 mol•L-1=10-amol•L-1,
可见酸中c(H+)与碱中c(OH-)相等,2Va=Vb混合后溶液的pH小于7,说明溶液呈酸性,应为弱酸与强碱的组合,
故答案为:酸是一种弱酸;
(2)酸中c(H+)=10-pH mol•L-1=10-amol•L-1,碱中c(OH-)=10pH-14 mol•L-1=10b-14 mol•L-1=10-(a+1)mol•L-1,pH=2时,c(H+)=10-2mol/L=$\frac{1{0}^{-1}mol/L×VL-1{0}^{-(a+1)}×0.05L}{VL+0.05L}$,解得:V=0.0111L=11.11mL,
故答案为:11.11;
(3)pH=b的某一元强碱溶液呈碱性,则b>7,
a=0.5b,则a>0.5×7=3.5,即a>$\frac{7}{2}$;
pH=a的强酸c(H+)=10-amol/L,pH=b的强碱c(OH-)=10b-14mol/L,恰好中和,则有Va×10-a=Vb×10b-14,
可得:$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14,
Va<Vb,则10a+b-14<1,即:a+b<14,又a=0.5b,则a+2a<14,
3a<14,则a<$\frac{14}{3}$,
所以:$\frac{7}{2}$<a<$\frac{14}{3}$,
故答案为:$\frac{7}{2}$<a<$\frac{14}{3}$.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握溶液pH的概念及表达式,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 周期表中原子半径最小的元素 |
| T | 最外层电子数是次外层电子数的3倍 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
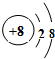 .
.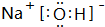 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\overline{v}$(NH3)=0.01 mol/(L•s) | B. | $\overline{v}$(O2)=0.00l0 mol/(L•s) | ||
| C. | $\overline{v}$(NO)=0.00l0 mol/(L•s) | D. | $\overline{v}$(H2O)=0.045 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径D>E>C>B | |
| B. | A、C、D、E四种元素形成的化合物溶于水一定显酸性 | |
| C. | C、D形成的化合物是离子化合物,只含有离子键 | |
| D. | A、C形成的化合物只有氧化性没有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生对Na2SO3与AgNO3在不同的pH下反应进行探究.
某学生对Na2SO3与AgNO3在不同的pH下反应进行探究.| 实验 | pH | 现 象 |
| a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
| b | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
| c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是指常温常压下,2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ | |
| B. | 是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),放出热量571.6 kJ | |
| C. | 是指标准状况下,2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ | |
| D. | 是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及 离子方程式 | 评 价 |
| A | 醋酸钠溶于水:CH3COO-+H2O═CH3COOH+OH- | 正确 |
| B | 实验室用浓盐酸与MnO2反应制Cl2: MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O | 错误,反应物中HCl电离出的H+、Cl-比例为1:1 |
| C | 硝酸铁溶液中加过量氨水:Fe3++3NH3•H2O═Fe(OH)3(胶体)+3NH4+ | 错误,Fe(OH)3应该是沉淀 |
| D | 铝溶于碳酸中:2Al+3H2CO3═2Al3++3H2+3 CO32- | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com