
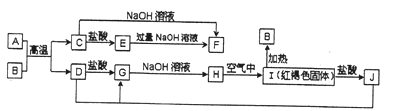
【题目】下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)。请回答下列问题:
(1)B的化学式为_______________。
(2)K的电子式为_________________。
(3)写出J与D反应转化为G的离子方程式___________________。
(4)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式_________________。
【答案】 Fe2O3 ![]() Fe+2Fe3+=3Fe2+ A1+2NaOH +2H2O =2NaAlO2 +3H2↑
Fe+2Fe3+=3Fe2+ A1+2NaOH +2H2O =2NaAlO2 +3H2↑
【解析】A和D为金属单质,固体条件下,金属和金属氧化物能发生铝热反应,则A是Al,C是Al2O3,Al2O3和盐酸反应生成AlCl3和水,AlCl3和NaOH溶液反应,所以E为AlCl3,Al2O3和AlCl3都与NaOH溶液反应生成NaAlO2,所以F是NaAlO2,H在空气中反应生成I,I为红褐色固体,则I为Fe(OH)3,H为Fe(OH)2,加热氢氧化铁固体生成Fe2O3和H2O,所以B是Fe2O3、K是H2O,氢氧化铁和盐酸反应生成FeCl3,所以J是FeCl3,根据元素守恒知,D是Fe,G是FeCl2。
(1)通过以上分析知,B是Fe2O3,故答案为:Fe2O3;
(2)K是H2O,水为共价化合物,氢原子和氧原子之间存在一对共用电子对,所以其电子式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)铁和氯化铁发生氧化还原反应生成氯化亚铁,离子反应方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】下表物质与其所含化学键类型、所属化合物类型完全正确的一组是
选项 | A | B | C | D |
物质 | CaCl2 | H2O2 | H2SO4 | NH4Cl |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键、共价键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 共价化合物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴奋剂是体育比赛中禁用的药物,曾获得2013年欧洲冬季锦标赛4×400米接力银牌的俄罗斯运动员科特尔雅洛娃,近日被查出使用含有兴奋剂成分的药物。有一种兴奋剂的结构如图。关于它的说法中不正确的是( )

A.该有机物能发生酯化反应
B.该有机物属于芳香烃
C.既能发生还原反应,又能发生氧化反应
D.1 mol 该物质最多跟5mol氢气发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是( )
A. 单质:生铁、赤铜、青铜
B. 有机物:甲烷、葡萄糖、乙醇
C. 纯净物:冰水混合物、纯碱、98%浓硫酸
D. 氧化物:双氧水、生石灰、烧碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示。下列说法不正确的是

A. 该反应的化学方程式为5A+4B![]() 4C
4C
B. 2min前,正反应速率逐渐减小,逆反应速率逐渐增大
C. 用B的浓度变化表示2min内的速率为2mol/(L·min)
D. 2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对相同质量的丙烯和乙烯的下列叙述中,错误的是
A. 碳原子个数比为1∶1B. 分子个数比为2∶3
C. 氢原子个数比为1∶1D. 分子个数比为3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两元素原子的L层电子数都是其他层电子总数的2倍,甲的原子半径大于乙的原子半径,下列说法正确是( )
A. 甲、乙处于同一周期 B. 它们中有一种元素位于第ⅥA族
C. 乙的最高价氧化物与甲的单质不反应 D. 简单甲离子的电子式为:Mg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com