
【题目】(1)FeCl3的水溶液呈___________(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):____________________________________________,
(2)实验室在配制好的FeCl3溶液中加少许稀盐酸的目的是:__________________ 。
(3)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是__________________ 。
【答案】酸 Fe3++3H2O ![]() Fe(OH)3+3H+ 抑制FeCl3的水解 Fe2O3
Fe(OH)3+3H+ 抑制FeCl3的水解 Fe2O3
【解析】
铁离子水解生成氢氧化铁和氢离子;盐酸可抑制铁离子水解,加热,促进氯化铁水解,生成的氯化氢容易挥发,据此分析解答。
(1)FeCl3为强酸弱碱盐,铁离子水解,溶液呈酸性,原因是:Fe3++3H2O![]() Fe(OH)3+3H+,故答案为:酸;Fe3++3H2O
Fe(OH)3+3H+,故答案为:酸;Fe3++3H2O![]() Fe(OH)3+3H+;
Fe(OH)3+3H+;
(2)实验室在配制好的FeCl3溶液中加少许稀盐酸,以抑制铁离子水解,故答案为:抑制FeCl3的水解;
(3)加热,促进氯化铁水解,生成的氯化氢容易挥发,因此将FeCl3溶液蒸干,得到氢氧化铁固体,灼烧,最后得到的主要固体产物是Fe2O3,故答案为:Fe2O3。


科目:高中化学 来源: 题型:
【题目】屠呦呦率领团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素。研究发现青蒿素中的某个基团对热不稳定,该基团还能与NaI作用生成I2 。碳原子连有4个不同的原子或基团时,该碳称为手性碳,下列分析不正确的是
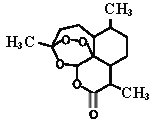
A. 推测青蒿素在乙醚中的溶解度大于在水中的溶解度
B. 青蒿素可以与NaOH、Na2CO3 、NaHCO3反应
C. 青蒿素分子中含有手性碳
D. 青蒿素中对热不稳定且具有氧化性的基团是“-O-O-”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生物电化学方法脱除水体中NH4+的原理如下图所示:
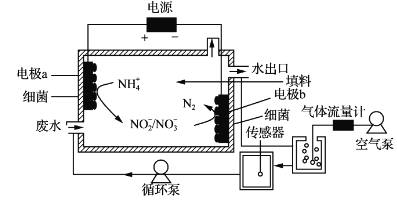
下列说法正确的是
A. 装置工作时,化学能转变为电能
B. 装置工作时,a极周围溶液pH降低
C. 装置内工作温度越高。NH4+脱除率一定越大
D. 电极b上发生的反应之一是:2NO3--2e-=N2↑+3O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予锂离子电池的发明者,锂离子电池是目前应用广泛的一类电池。以钛铁矿(主要成分为FeTiO3,含有少量MgO、Fe2O3、SiO2等杂质)为原料,制备锂离子电池电极材料的工艺流程如图所示:
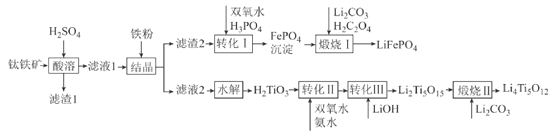
已知:①滤液1中含Ti微粒的主要存在形式为TiO2+;
②)Ksp(FePO4)=1.3×10-22、Ksp[Mg3(PO4)2]=1.0×10-24;溶液中某离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。
请回答下列问题:
(1)滤渣1中主要成分的化学式为__。
(2)“结晶”温度需控制在70℃左右,若温度过高会导致的后果为__。
(3)“转化I”后所得溶液中c(Mg2+)=0.01mol·L-1,若其中Fe3+沉淀完全,则溶液中c(PO43-)的范围为__。
(4)“煅烧I”反应中氧化剂和还原剂的物质的量之比为__。
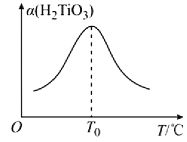
(5)“转化II”中H2TiO3的转化率(α)与温度(T)的关系如图所示。T0℃时,一定时间内H2TiO3的转化率最高的原因为__。
(6)Li2Ti5O15中-1价与-2价O原子的数目之比为___。“煅烧II”反应中同时生成两种参与大气循环的气体,该反应的化学方程式为__。
(7)某锂离子电池放电时的电池反应为Li1-xFePO4+LixC6=LiFePO4+6C,则充电时阳极的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研团队研制出“TM﹣LiH(TM表示过渡金属)”双催化剂体系,显著提高了在温和条件下氮气和氢气合成NH3的效率,原理示意如下:

下列分析不合理的是( )
A.状态Ⅰ,吸收能量并有N≡N键发生断裂B.合成NH3总反应的原子利用率是100%
C.“TM﹣LiH”能降低合成氨反应的△HD.生成NH3:2LiNH+3H2═2LiH+2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.1000mol/L NaOH标准溶液。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.1000 | 30.05 | 20.00 |
2 | 0.1000 | 29.95 | 20.00 |
3 | 0.1000 | 28.20 | 20.00 |
①滴定达到终点的判断是________,此时锥形瓶内溶液的pH为_____________。
②根据上述数据,可计算出该盐酸的浓度约为___________(保留四位有效数字)
③排去碱式滴定管中气泡的方法应采用操作__________,然后轻轻挤压玻璃球使尖嘴部分充满碱液
甲.![]() 乙.
乙.![]() 丙.
丙.![]()
④在上述实验中,下列操作(其他操作正确)会造成盐酸浓度测定结果偏高的有_____
A、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
B、锥形瓶水洗后未干燥
C、滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D、配制NaOH标准溶液时,移液后未洗涤烧杯和玻璃棒
E、碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示不正确的是
A.葡萄糖的最简式:CH2O
B.次氯酸的结构式:H-O-Cl
C.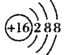 可以表示32S2- ,也可以表示34S2-
可以表示32S2- ,也可以表示34S2-
D.![]() 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气和金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解,受热易升华。装置如下:
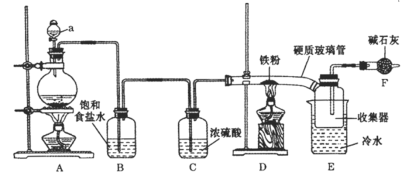
(1)仪器a的名称是____________。
(2)A中反应的离子方程式是__________,D中反应的化学方程式是__________。
(3)反应开始时,先点燃____________处的酒精灯(填“A”或“D”)。
(4)若无B、C两装置,所得产物中可能含有的杂质是_____________(写化学式)。
(5)F中碱石灰的作用是____________(写2点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含![]() 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
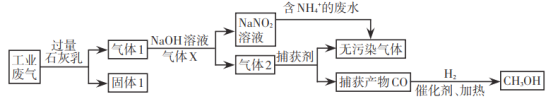
已知:1 mol CO和1 mol CH3OH分别完全燃烧生成CO2(g)和H2O(l),放出的热量为283.0kJ和726.5kJ。下列说法错误的是
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.气体X在流程中体现还原性
C.相同质量的CO和CH3OH完全燃烧,后者放出的热量多
D.处理含![]() 废水时,发生反应的离子方程式为:
废水时,发生反应的离子方程式为:![]() +
+![]() =N2↑+2H2O
=N2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com