
| A. | 0.044mol/L | B. | 0.44mol/L | C. | 4.4mol/L | D. | 44mol/L |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| C. | 蛋白质、淀粉、纤维素都属于有机高分子化合物 | |
| D. | 天然纤维和合成纤维的主要成分是纤维素 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑦ | B. | ②④⑤⑦ | C. | ④⑤ | D. | ①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
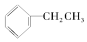 ⑤CH3COOCH3 ⑥
⑤CH3COOCH3 ⑥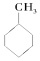
| A. | ②③⑤ | B. | ①⑤⑥ | C. | ①④⑥ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,活化分子百分数增大,正、逆反应速率都加快 | |
| B. | 使用催化剂,活化分子百分数增大,正、逆反应速率都加快 | |
| C. | 使用催化剂可以降低反应的活化能 | |
| D. | 升高温度,上述反应的平衡常数会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 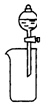 从Mg(OH)2悬浊液中分离出Mg(OH)2 | B. | 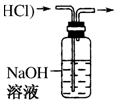 除去HCl中的SO2 | ||
| C. | 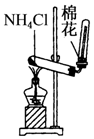 实验室制氨气 | D. | 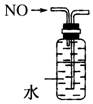 排水法收集NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com