
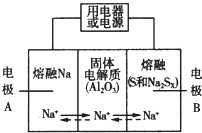
 �����������ڽ���Na������S�Ͷ����ƣ�Na2SX���ֱ���Ϊ�����缫�ķ�Ӧ������Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ��ʾ��
�����������ڽ���Na������S�Ͷ����ƣ�Na2SX���ֱ���Ϊ�����缫�ķ�Ӧ������Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ��ʾ��| ���� | Na | S | Al2O3 |
| �۵�/�� | 97.8 | 115 | 2050 |
| �е�/�� | 892 | 444.6 | 2980 |
���� ��1��ԭ��ع���ʱ�����Ƶ��¶�ӦΪ����Na��SΪ����״̬��
��2��Na��������ӦΪԭ��ظ������������������ƶ������ʱ��������ӦΪԭ���������Ӧ���淴Ӧ��Ӧ����S���Դ˽��
��3�����NaCl��Һ�ķ�ӦʽΪ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����ÿ����2molNaOHת�Ƶ���2mol������Һ��pH��Ϊl3ʱ��c��OH-��=0.1mol/L������NaOH���ʵ���Ϊ0.05mol��ת�Ƶ���0.05mol����ת�Ƶ��������������仯��
��� �⣺��1��ԭ��ع���ʱ�����Ƶ��¶�ӦΪ����Na��SΪ����״̬�����¶�Ӧ����115�������444.6�棬ֻ��c���ϣ��ʴ�Ϊ��C��
��2��A���ŵ�ʱ��Na��������ӦΪԭ��ظ�������A��ȷ��
B���������������ƶ�������A��B����B����
C��AΪ�������ŵ�ʱ����������Ӧ�����ʱ������ԭ��Ӧ���ӵ�Դ��������C����
D�����ʱ���ǵ��ط�Ӧ��BΪ������������ӦΪ��Sx2--2e-=xS����D��ȷ��
�ʴ�Ϊ��AD��
��3�����NaCl��Һ�ķ�ӦʽΪ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����ÿ����2molNaOHת�Ƶ���2mol������Һ��pH��Ϊl3ʱ��c��OH-��=0.1mol/L������NaOH���ʵ���Ϊ0.05mol��ת�Ƶ���0.05mol��ת��0.05mol���ӣ�����Na��������1.15g�����������仯1.15g�������ķ�Ӧ���������Ϊ2.3g���ʴ�Ϊ��0.05��2.3��
���� ���⿼��ԭ���֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬ע�����ԭ��صĹ���ԭ���Լ��缫����ʽ����д������ʱע����ᣬ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ϡ����ϳ���ά����ȩ��֬�������л��߷��ӻ����� | |
| B�� | ���������Na2SO4��CuSO4������������������ | |
| C�� | ��֬��������Ӧ���ɸ�֬����ͱ��� | |
| D�� | ͨ��ʯ�ʹ������ǻ��ϩ������Ҫ;�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
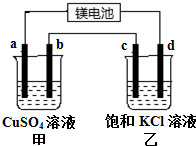 ��һ��þ���ε�أ���ӦΪ��xMg+Mo3S4$?_{���}^{�ŵ�}$MgxMo3S4�����Ӽס���װ�ý��е�⣮��ͼ��ʾ��a��b��c��Ϊʯī�缫��dΪFe�缫�����ʱd��������ų�������˵������ȷ���ǣ�������
��һ��þ���ε�أ���ӦΪ��xMg+Mo3S4$?_{���}^{�ŵ�}$MgxMo3S4�����Ӽס���װ�ý��е�⣮��ͼ��ʾ��a��b��c��Ϊʯī�缫��dΪFe�缫�����ʱd��������ų�������˵������ȷ���ǣ�������| A�� | ��װ����a�ĵ缫��ӦΪ4OH--4e-�TO2��+2H2O | |
| B�� | �ŵ�ʱþ��������ĵ缫��ӦΪ Mo3S4+2xe-�TMo3S42x- | |
| C�� | ��d������0.56 L����״��������ʱ��b������3.2 g | |
| D�� | þ��طŵ�ʱ���׳��е�SO42-����a�缫 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˵���ǽ�����Cl��C��2HClO3+CaCO3=Ca��ClO3��2+CO2��+H2O | |
| B�� | ��˵��������H2O2��Fe3+��2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C�� | ��Na2S2O3��Һ��ͨ������������S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ | |
| D�� | Ǧ�����س��ʱ�ĸ�����Ӧ��PbSO4+2H2O-2e-=PbO2+4H++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������Ϊ37����ԭ�ӣ�${\;}_{37}^{17}$Cl | B�� | Al3+�Ľṹʾ��ͼ��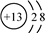 | ||
| C�� | NaClO�ĵ���ʽ��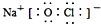 | D�� | �������Ľṹ��ʽ��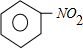 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
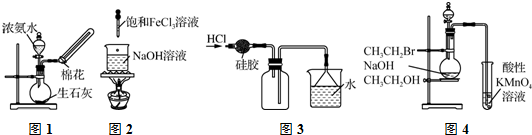
| A�� | ����ͼ1��ʾװ����ȡ����NH3 | |
| B�� | ����ͼ2��ʾװ���Ʊ�Fe��OH��3���� | |
| C�� | ����ͼ3��ʾװ���ռ�HCl | |
| D�� | ����ͼ4��ʾװ�ü����Ƿ�������ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ�� pH=4 | |
| B�� | �����¶ȣ���Һ�� pH ���� | |
| C�� | ����ĵ���ƽ�ⳣ��ԼΪ 1��10-7 | |
| D�� | �� HA ������� c��H+��ԼΪˮ������� c��H+����106�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com