
【题目】有一类物质可表示为Al2O3·2SiO2·2H2O,这类物质是一种
A.混合物B.含氧酸C.硅酸盐D.铝酸盐
科目:高中化学 来源: 题型:
【题目】科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于
A. 揭示了燃烧的本质B. 提出了元素周期律
C. 开发了合成氨的生产工艺D. 提取了治疟药物青蒿素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述相符的是( ) 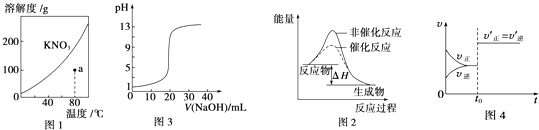
A.图1表示KNO3的溶解度曲线,图中a点对应的溶液是80℃时KNO3的饱和溶液
B.图2表示某吸热热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000 molL﹣1 NaOH溶液滴定20.00 mL 0.1000 molL﹣1醋酸溶液的滴定曲线
D.图4表示t0时改变的条件可能是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+B(g) ![]() 2C(g),根据下表中的数据判断下列图象错误的是( )
2C(g),根据下表中的数据判断下列图象错误的是( )
| p1(Mpa) | p2(Mpa) |
400℃ | 99.6 | 99.7 |
500℃ | 96.9 | 97.8 |
A.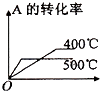
B.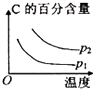
C.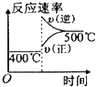
D.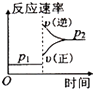
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 油脂中的碳链为碳碳单键时主要是低沸点的植物油
B. 油脂是产生能量最高的营养物质
C. 脂肪在人体内水解生成甘油和高级脂肪酸
D. 油脂能增进食欲但是如果摄入过量能够引起很多疾病
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳和氨是重要的化工产品,是纯碱工业、制造硝酸、铵盐和氮肥等的原料.
(1)CO2的电子式是 .
(2)以NH3与CO2为原料合成尿素[化学式为CO(NH2)2]的主要反应如下:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=﹣l59.5kJmol﹣1
②NH2CO2NH4(s)CO(NH2)2(s)+H2O(g)△H=+116.5kJmol﹣1
③H2O(1)═H2O(g)△H=+44.0kJmol﹣1
写出CO2与NH3合成尿素和液态水的热化学反应方程式;
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣905kJmol﹣1不同温度下NO产率如下图1所示,由此图可知温度对NO产率的影响规律为 , 请用化学反应速率和化学平衡理论解释其原因: . 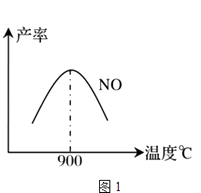
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如图2所示,在使用过程中石墨I电极反应生成一种氧化物Y,有关石墨I电极反应可表示为 . 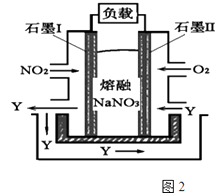
(5)已知常温下NH3H2O的电离平衡常数K=1.75×10﹣5 , H2CO3的电离平衡常数K1=4.4×10﹣7 , K2=4.7×10﹣11 . 常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显(填“酸性”、“中性”或“碱性”);计算反应NH4++HCO3﹣+H2ONH3H2O+H2CO3的平衡常数K=(结果保留2位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是生产羰基化学品的基本原料,对于以水煤气为原料提取CO的工艺,如果氢气
未能充分利用,则提高了CO生产成本,所以在煤化工中常需研究不同温度下的平衡常数、投料比及热值问题.反应CO(g)+H2O (g)H2(g)+CO2(g)的平衡常数随温度的变化如表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | a |
(1)上述反应的逆反应是(填“放热”或“吸热”)反应.
(2)已知在一定温度下:C(s)+CO2(g)2CO(g) K
C(s)+H2O (g)H2(g)+CO(g) K1
CO(g)+H2O (g)H2(g)+CO2(g) K2
则K、K1、K2、之间的关系是 .
(3)800℃时,在2L的恒容密闭容器中,充入2.0molCO(g)和3.0molH2O(g),保持温度不变进行反应:CO(g)+H2O (g)H2(g)+CO2(g),4min时反应达到平衡,测得CO的转化率为60%.
①0~4min内,CO2的平均反应速率为molL﹣1min﹣1 , 800℃时a= .
②800℃时四个不同容器中发生上述反应,测得各物质的浓度(molL﹣1)如表,其中达到平衡状态的是(填字母).
A | B | C | D | |
c(CO2) | 3 | 1 | 0.8 | 1 |
c(H2) | 2 | 1 | 0.8 | 1 |
c(CO) | 1 | 2 | 3 | 0.5 |
c(H2O) | 2 | 2 | 3 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com