
 ,以此确定烯烃.
,以此确定烯烃. ,故答案为:
,故答案为: ;
; ,烃A可能有的结构简式为(CH3)3C-CH=CH2、CH3-C(CH3)=C(CH3)-CH3、CH3CH(CH3)-C(CH3)=CH2等,
,烃A可能有的结构简式为(CH3)3C-CH=CH2、CH3-C(CH3)=C(CH3)-CH3、CH3CH(CH3)-C(CH3)=CH2等,

 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
A、2NaCl+H2SO4(浓)
| ||||
B、Cu+2H2SO4(浓)
| ||||
C、C+2H2SO4(浓)
| ||||
D、Fe2O3+3H2SO4(浓)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇的结构简式:C2H6O | ||||
B、CH4的比例模型: | ||||
C、工业上制取粗硅的化学方程式:SiO2+C
| ||||
| D、电解饱和食盐水的离子方程式:Cl-+2H2O═Cl2↑+2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子晶体中一定存在分子间作用力,不一定存在共价键 |
| B、H2O沸点高于NH3,是因为H2O分子间存在氢键而NH3分子间不存在氢键 |
| C、含有金属离子的晶体一定是离子晶体 |
| D、二氧化硅的结构式:Si=O=Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、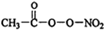 (PAN)等二次污染物.
(PAN)等二次污染物.| m |
| n |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图Ⅰ、Ⅱ、Ⅲ所示装置进行有关实验,将A逐滴加入B中.
如图Ⅰ、Ⅱ、Ⅲ所示装置进行有关实验,将A逐滴加入B中.| 浓硫酸 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
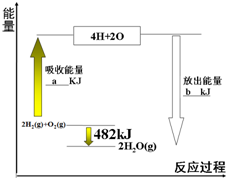 拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:
拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:| 共价键 | H-H | O=O | H-O |
| 键能/kJ?mol-1 | 436 | 498 | X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com