
| A. | 盐:Ca(ClO)2 NH4NO3 K2SiO3 | |
| B. | 酸性氧化物:Al2O3 K2O CO2 | |
| C. | 电解质:HCl Ba(OH)2 CO | |
| D. | 非电解质:Cl2 NO 乙醇(C2H5OH) |
分析 水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;酸性氧化物是能和碱反应生成盐和水的氧化物;盐是由金属阳离子或铵根离子与酸根离子构成的化合物;在水溶液中和熔融状态下都不能够导电的化合物是非电解质.
解答 解:A、Ca(ClO)2、NH4NO3、K2SiO3都是能电离出金属阳离子(铵根离子)和酸根阴离子的化合物,属于盐,故A正确;
B、Al2O3、K2O、CO2分别属于两性氧化物、碱性氧化物、酸性氧化物,故B错误;
C、HCl、Ba(OH)2属于电解质,CO属于非电解质,故C错误;
D、Cl2既不是电解质又不是非电解质,NO、乙醇(C2H5OH)属于非电解质,故D错误.
故选A.
点评 本题考查了电解质、盐、氧化物的概念及其联系,难度不大,但概念间的联系是学习的难点,属于易错题.


科目:高中化学 来源: 题型:选择题
| A. | 上述反应中硫元素只被氧化 | |
| B. | Na2S2O3在强酸性环境中能稳定存在 | |
| C. | 每生成1 molNa2S2O3,转移电子数为4NA | |
| D. | 若将Na2CO3换成Na2SO3(配比不变),每吸收3 molSO2,理论上就会生成3mol Na2S2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在铜锌原电池中,铜作负极 | |
| B. | 在铜锌原电池中,锌作阴极 | |
| C. | 原电池是将化学能转化为电能的装置 | |
| D. | 原电池是将电能转化为化学能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CH3COOC2H5+H2O,反应类型酯化反应(取代反应).
CH3COOC2H5+H2O,反应类型酯化反应(取代反应).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的是七个基本物理量之一 | B. | 阿伏加德罗常数是没有单位的 | ||
| C. | 1mol氮气的体积是22.4L | D. | 1mol H2O含有1个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4L乙烯中C-H键数为4NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
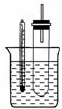 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 上述现象说明[Cu(NH3)4]2+不如Cu(OH)2稳定 | |
| D. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 人造羊毛的主要成分为聚丙烯腈
人造羊毛的主要成分为聚丙烯腈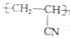 ,此物质可由以下三种途径合成,已知A是石油分馏的一种产品.
,此物质可由以下三种途径合成,已知A是石油分馏的一种产品. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com