
下列说法不正确的是
A.探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合
B.用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值
C.H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快
D.欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高一上段考化学试卷(解析版) 题型:选择题
在常温下发生下列反应:
①16H+ + 10Z—+ 2XO4— = 2X2+ + 5Z2 + 8H2O
②2A2+ + B2 = 2A3+ + 2B—
③2B—+ Z2 = B2 + 2Z—
根据上述反应,判断下列结论中错误的是
A.溶液中可能发生反应:Z2 + 2A2+ = 2A3+ + 2Z—
B.Z在①③反应中作还原剂
C.氧化性强弱顺序为XO4—>Z2>B2>A3+
D.X2+ 是XO4— 的还原产物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高二上期中考试化学试卷(解析版) 题型:选择题
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液浓度和混合所得溶液的pH如下表所示:
实验编号 | c(HA)/ mol·L-1 | c(NaOH)/ mol·L-1 | 混合液的pH |
① | 0.2 | 0.1 | pH>7 |
② | c | 0.2 | pH=7 |
③ | 0.1 | 0.1 | pH=9 |
下列说法中,不正确的是
A.由实验①可知,HA为弱酸;
B.实验① 所得混合溶液:c(Na+)>c(A-)>c(OH-)>c(H+)
所得混合溶液:c(Na+)>c(A-)>c(OH-)>c(H+)
C.实验②所得混合溶液:c(Na+)=c(A-)
D.实验③所得混合溶液中由水电离出的OH-的浓度为1×10-9 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
在日常生活中出现了“加碘食盐”“增铁酱油”“高钙牛奶”“富硒茶叶”“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为( )
A.元素 B.单质 C.分子 D.氧化物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:选择题
对于物质的量浓度均为0.01 mol/L的①NaHCO3、②Na2CO3、③CH3COOH、④CH3COONa四种溶液,下列说法正确的是
A.①的离子浓度为:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
B.②c(OH﹣)=c(HCO3﹣)+c(H+)+c(H2CO3)
C.③加入等体积的水稀释,电离平衡正向移动,c(H+)增大
D.④和③等体积混合,c(CH3COO-)+c(CH3COOH)=0.01 mol/L
查看答案和解析>>
科目:高中化学 来源:2016届云南师大附中高考适应性月考(四)理综化学试卷(解析版) 题型:填空题
淡水是一种重要的自然资源,是人类赖以生存不可缺少的物质。按要求回答下列问题:
(1)水质优劣直接影响人体健康。天然水在净化处理过程中加入的混凝剂可以是___________(填一种物质的名称),其净水作用的原理是_________________________ ____。混凝剂难以清除溶解于水中的有机物、无机物、微生物,混凝剂沉淀后还需要_____________。
(2)硬水的软化指的是_________________________ ____________________________ ___。
(3)硬度为1°的水是指每升水含10mg CaO或与之相当的物质(如7.1mg MgO)。若某天然水中c(Ca2+)=1.2×10-3mol/L,c(Mg2+)=6×10-4mol/L,则此水的硬度为_____________。
(4)若(3)中的天然水还含有c(HCO3-)=8×10-4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2____________g, 后加入Na2CO3___________g 。
(5)如图是电渗析法淡化海水的原理图,其中,电极A接直流电源的正极,电极B接直流电源的负极。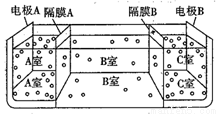
①隔膜A是_________(填“阴”或“阳”)离子交换膜。
②某种海水样品,经分析含有大量的Na+、Cl-,以及少量的K+、SO42-。若用上述装置对该海水进行淡化,当淡化工作完成后,A、B、C三室中所得溶液(或液体)的pH分别为pHa、pHb、pHc,则其大小顺序为________________________。
查看答案和解析>>
科目:高中化学 来源:2016届四川成都第七中学高三阶段测试三理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.10mL20mol/L浓硫酸与足量锌反应,转移电子数为0.2NA
B.0.1mol24Mg18O晶体中所含中子总数为2.0NA
C.在标准状况下,2.8gN2和2.24LCO所含电子数均为1.4NA
D.1L1mol/L的NaClO溶液中含有ClO-的数目为NA
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:选择题
化学科学对提高人类生活质量和促进社会发展具有重要作用,下列说法正确的是
①汽车尾气的大量排放影响了空气的质量,但是不会造成PM2.5值升高
②研发安全特效药物,有利于人类抵御疾病
③规范食品添加剂的生产并科学使用,有利于保障人体健康和生命安全
④推广城市生活垃圾处理的减量化、资源化、无害化技术,有利于环境保护和资源充分利用
⑤用聚氯乙烯代替聚乙烯作食品包装袋,有利于节约使用成本
A.②③④ B.②④⑤ C.①③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:填空题
(1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示。试回答:
AB段曲线所表示的反应化学方程式是: 。

将B处生成的溶液煮沸,反应化学方程式是: 。
(2)已知硫可与热的KOH溶液发生反应,反应方程式如下:3S+6KOH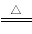 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
据此回答以下问题:
①在上述反应中,氧化剂与还原剂的物质的量之比为 。
②在上述反应中,若有3 mol硫单质参与反应,则转移电子的物质的量是 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com