
【题目】科研人员设想用如图所示装置生产硫酸,下列说法正确的是( ) 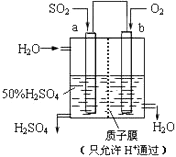
A.a为正极,b为负极
B.负极反应式为2H2O+SO2﹣2e﹣=SO42﹣+4H+
C.电子从b极向a极移动
D.生产过程中H+由b电极区通过质子膜向a电极区运动
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用.氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题: 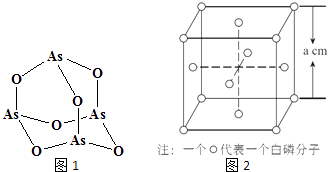
(1)As原子的核外电子排布式为 .
(2)P和S是同一周期的两种元素,P的第一电离能比S大,原因是 .
(3)NH4+中H﹣N﹣H的键角比NH3中H﹣N﹣H的键角(填“大”或“小”),原因是 .
(4)Na3AsO4中含有的化学键类型包括;AsO43﹣的空间构型为 , As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是 .
(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5是晶体.
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol﹣l , 则该晶胞中含有的P原子的个数为 , 该晶体的密度为gcm﹣3(用含NA、a的式子表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有氧化铁和氧化铜的混合物m g,向其中加入100mL 3mol·L-1硝酸,恰好完全溶解,若m g该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为 ( )
A. (m-1.6)g B. (m-2.4)g C. (m-3.2)g D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( )
A.ΔH=+244.1 kJ/mol B.ΔH=-488.3 kJ/mol
C.ΔH=-996.6 kJ/mol D.ΔH=+996.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1molL﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2 molL﹣1盐酸
D.提高溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.为了研究化学反应A+B![]() C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
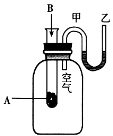
试回答下列问题:
(1)该反应为_______反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)物质中的化学能通过化学反应转化成_______释放出来。
(4)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:_____________________。
Ⅱ.同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。
已知:
P4(白磷,s)+5O2(g)![]() P4O10(s) ΔH=2983.2 kJ·mol1 ①
P4O10(s) ΔH=2983.2 kJ·mol1 ①
P(红磷,s)+ ![]() O2(g)
O2(g)![]()
![]() P4O10(s) △H=738.5 kJ·mol1 ②
P4O10(s) △H=738.5 kJ·mol1 ②
则白磷转化为红磷的热化学方程式为______________。相同状况下,能量状态较低的是_______;白磷的稳定性比红磷_______(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的书写及对应表述均正确的是
A.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g 时,放出19.12 kJ 热量。则Fe(s)+S(s)![]() FeS(s) △H=95.6 kJmol1
FeS(s) △H=95.6 kJmol1
B.足量稀醋酸与 0.1 molL1NaOH 溶液反应:H+(aq)+OH(aq) ![]() H2O(l) △H=57.3 kJmol1
H2O(l) △H=57.3 kJmol1
C.已知,1 mol H2完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为:2H2O(l)![]() 2H2(g)+O2(g) △H=285.5kJmol1
2H2(g)+O2(g) △H=285.5kJmol1
D.已知 2C(s)+O2(g)![]() 2CO(g) △H= 221kJmol1,则可知 C 的燃烧热△H=110.5 kJmol1
2CO(g) △H= 221kJmol1,则可知 C 的燃烧热△H=110.5 kJmol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,下列物质占体积最大的是( )。
A. 64g H2O B. 6.02×1023个氮分子 C. 44.8L HCl D. 6g氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池和电解池都能实现能量的置换.回答下列问题:
(1)可将化学能转化为电能是池;
(2)下列反应能设计成原电池的是:
①2FeCl3+Fe═3FeCl2 . Com]
②AlCl3+3NH3H2O═Al(OH)3↓+3NH4Cl
③NaOH+HCl═NaC1+H2O
(3)用FeCl3溶液腐蚀印刷电路铜板的离子方程式为:
(4)如图装置当闭合电键时,电表显示有电流通过.则Pt极的电极反应式:当甲中产生0.1mol气体时,乙中析出铜的质量应为g. 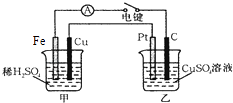
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com