
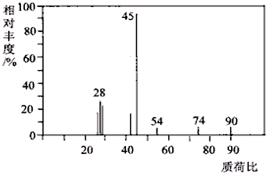
 有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.
有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.| 5.4g |
| 18g/mol |
| 13.2g |
| 44g/mol |
| 4.8g |
| 16g/mol |
 、1个-OH,有机物A的结构简式为CH3CH(OH)COOH,故答案为:CH3CH(OH)COOH;
、1个-OH,有机物A的结构简式为CH3CH(OH)COOH,故答案为:CH3CH(OH)COOH; ,由方程式可知0.1molA与足量Na反应生成氢气0.1mol,在标准状况下产生H2的体积是0.1mol×22.4L/mol=2.24L,
,由方程式可知0.1molA与足量Na反应生成氢气0.1mol,在标准状况下产生H2的体积是0.1mol×22.4L/mol=2.24L,

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 |  |  | … |
| 1 | 2 | 3 | … |
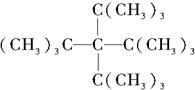
| A、C23H48 |
| B、C33H68 |
| C、C43H88 |
| D、C53H108 |
查看答案和解析>>
科目:高中化学 来源: 题型:
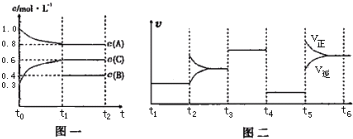
| A、此温度下该反应的化学方程式2A(g)+B(g)?2C(g) | ||||
| B、t4~t5阶段改变的条件为减小压强 | ||||
| C、B 的起始物质的量为1.0mol | ||||
D、在相同条件下,若起始时容器中加入amol A、bmol B 和cmol C,要达到 t1时刻同样的平衡,a、b、c 要满足的条件为a+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 | B、17 | C、23 | D、31 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.68 g |
| B、5.58 g |
| C、2.34 g |
| D、2.34 mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com