
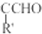
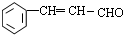 .
.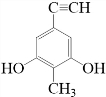 等.(任写一种)
等.(任写一种)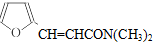 )是一种高效麻醉剂,写出以
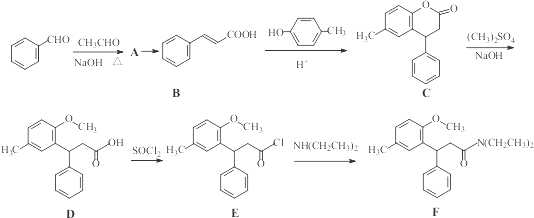
)是一种高效麻醉剂,写出以 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:分析 (1)由D的结构简式可知,含有的含氧官能团为羧基、醚键;
对比B、C结构可知,B与对甲基苯酚发生酯化反应,甲基间位的C-H键断裂与碳碳双键发生加成反应形成六元环;
(2)由信息可知,对比苯甲醛与乙醛反应得到A为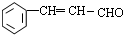 ;
;
(3)苯甲醛与银氨溶液反应氧化反应得到苯甲酸铵、Ag、氨气与水;
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色,说明含有不饱和键,可以是碳碳三键等,②能与FeCl3溶液发生显色反应,说明含有酚羟基,结合分子中有4种不同化学环境的氢书写;
(5) 与CH3CHO在氢氧化钠、加热条件下得到
与CH3CHO在氢氧化钠、加热条件下得到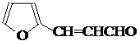 ,再用新制氢氧化铜氧化、然后酸化得到
,再用新制氢氧化铜氧化、然后酸化得到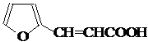 ,再与SOCl2发生取代反应得到
,再与SOCl2发生取代反应得到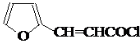 ,最后与NH(CH3)2反应得到
,最后与NH(CH3)2反应得到 .
.
解答 解:(1)由D的结构简式可知,含有的含氧官能团为羧基、醚键;
对比B、C结构可知,B与对甲基苯酚发生酯化反应,属于取代反应,甲基间位的C-H键断裂与碳碳双键发生加成反应形成六元环,
故答案为:羧基、醚键;取代反应、加成反应;
(2)由信息可知,对比苯甲醛与乙醛反应得到A为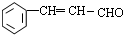 ,
,
故答案为: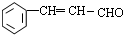 ;
;
(3)苯甲醛与银氨溶液反应氧化反应得到苯甲酸铵、Ag、氨气与水,反应方程式为:,
故答案为:;
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色,说明含有不饱和键,可以是碳碳三键等,②能与FeCl3溶液发生显色反应,说明含有酚羟基,③分子中有4种不同化学环境的氢,符合条件的同分异构体有: 、
、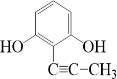 等,
等,
故答案为: 等;
等;
(5) 与CH3CHO在氢氧化钠、加热条件下得到
与CH3CHO在氢氧化钠、加热条件下得到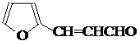 ,再用新制氢氧化铜氧化、然后酸化得到
,再用新制氢氧化铜氧化、然后酸化得到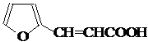 ,再与SOCl2发生取代反应得到
,再与SOCl2发生取代反应得到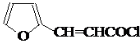 ,最后与NH(CH3)2反应得到
,最后与NH(CH3)2反应得到 ,合成路线流程图:
,合成路线流程图: ,
,
故答案为: .
.
点评 本题考查有机物的合成与推断、官能团的结构与性质、有机反应类型、限制条件同分异构体书写等,注意利用转化关系中隐含信息进行合成路线设计,较好的考查学生信息获取与知识迁移运用能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | NaHCO3溶液中加入足量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 钠和水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属单质中一定存在共价键 | |
| B. | 含共价键的化合物一定是共价化合物 | |
| C. | 含离子键的化合物一定是离子化合物 | |
| D. | 溶于水能导电的化合物就是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | N原子的第一电离能小于O原子 | 同周期元素原子的电离能随原子序数增大而增大 |
| B | CO2为直线形分子 | CO2分子中C为sp杂化,键角为180° |
| C | 金刚石的熔点高于石墨 | 金刚石是原子晶体,石墨是分子晶体 |
| D | HF的沸点低于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.01mol•L-1Ba(OH)2溶液中:Na+、NH4+、NO3-、HCO3- | |
| B. | 使甲基橙变红色的溶液中:Mg2+、Fe2+、NO3-、Cl- | |
| C. | pH=7的溶液中:K+、Cl-、Br-、Fe3+ | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、I-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 既能与酸反应,又能与碱反应 | |
| B. | 导电性好 | |
| C. | 熔点低 | |
| D. | 具有还原性,在冶炼反应中放出大量的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①③⑥ | C. | ②③④ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子.
已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子.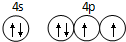 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com