


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 3 mol?L-1的KCl溶液 |
| B、75 mL 2.5 mol?L-1的CaCl2溶液 |
| C、150 mL 3 mol?L-1KClO3溶液 |
| D、25 mL 2 mol?L-1的FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用盐酸酸化的BaCl2溶液来判断亚硫酸钠固体是否发生变质 |
| B、实验室用加热NH4Cl的方法来制取氨气 |
| C、可加入足量的铜粉然后过滤来除去氯化亚铁溶液中的少量氯化铁 |
| D、加入澄清石灰水看是否有白色沉淀来区别碳酸钠溶液和碳酸氢钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
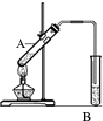 (1)实验室用右图所示装置制取乙酸乙酯,在试管A中加入的试剂有无水酒精、浓硫酸和冰醋酸(CH3COOH).请写出该反应的化学方程式)
(1)实验室用右图所示装置制取乙酸乙酯,在试管A中加入的试剂有无水酒精、浓硫酸和冰醋酸(CH3COOH).请写出该反应的化学方程式)查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 分析化学中常用X射线研究晶体的结构.有一种晶体KxFey(CN)z,其中Fe2+、Fe3+、CNˉ的排布如图所示,其中Fe2+和Fe3+位于立方体的顶点,自身互不相邻,CNˉ位于立方体的棱上,每隔一个立方体,在立方体的中心含有一个K+(未画出).
分析化学中常用X射线研究晶体的结构.有一种晶体KxFey(CN)z,其中Fe2+、Fe3+、CNˉ的排布如图所示,其中Fe2+和Fe3+位于立方体的顶点,自身互不相邻,CNˉ位于立方体的棱上,每隔一个立方体,在立方体的中心含有一个K+(未画出).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管将多余液体吸出即可 |
| B、用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ |
| C、区别FeCl3溶液和Fe(OH)3胶体时,可将它们分别用一束光照射,看有无丁达尔效应出现 |
| D、检验某溶液中是否含有Fe3+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com