
已知Cr2O72-、Cr3+、CH3CH2OH、CH3COOH、H+、H2O六种微粒属于一个氧化还原反应中的反应物和生成物。下列叙述中不正确的是
A.还原产物为CH3COOH
B.氧化剂与还原剂的物质的量之比为2:3
C.Cr2O72-和Cr3+分别属于反应物和生成物
D.若把该反应设计从成原电池,则负极反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+
科目:高中化学 来源:2016-2017学年辽宁省高二上10月月考化学试卷(解析版) 题型:选择题
已知25℃、101kPa条件下:
4Al(s)+3O2(g)=2Al2O3;△H=-2834.9kJ·mol-1
4Al(s)+2O3(g)=2Al2O3;△H=-3119.1kJ·mol-1
由此得出的正确结论是
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应
D.O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第二次月考化学试卷(解析版) 题型:选择题
将1.95 g锌粉加入到200 mL 0.1 mol·L-1的MO2+溶液中,恰好完全反应,其他物质忽略,则还原产物可能是( )
A.M2+ B.M
C.M3+ D.MO2+
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:实验题
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中,从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,能加快溶出率的操作有 、 。(写出两条)
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴,则浸出钴的离子反应方程式为 (产物中只有一种酸根)。请从反应原理分析不用盐酸浸出钴的主要原因 。
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: ; 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
将一定体积的CO2通入VLNaOH溶液中,已知反应物均无剩余。若在反应后的溶液中加入足量石灰水,得到ag沉淀;若在反应后的溶液中加入足量CaCl2溶液,得到bg沉淀,则下列说法正确的是
A.参加反应的CO2的体积为0.224aL
B.若a=b,则CO2与NaOH溶液反应的产物盐只有Na2CO3
C.用上述数据不能确定NaOH溶液的物质的量浓度
D.a可能等于、小于或大于b
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数的值,下列说法正确的是
A.0.1molCl2溶于足量水中,转移的电子数为0.1NA
B.100g98%的浓硫酸中,氧原子总数为4NA
C.常温常压下,3g甲醛所含σ键数目为0.3NA
D.1molFeCl3与沸水反应生成胶体后,含有的Fe(OH)3胶粒数目为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上第一次月考化学试卷(解析版) 题型:实验题
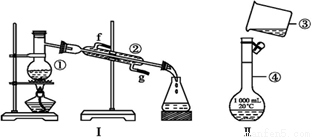
(1)写出下列仪器的名称:
① ,② ,④ 。
(2)仪器①~④中,使用时必须检查是否漏水的是 (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是 ,将仪器补充完整后进行的实验操作的名称为 ;②的进水口是 (填“f”或“g”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上第一次月考化学试卷(解析版) 题型:选择题
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上10月月考化学试卷(解析版) 题型:选择题
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热的ΔH分别是
“嫦娥一号”发射火箭燃料 | 液氢 (H2) | ① 2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 ②2H2 (l)+O2(l) =2H2O(g) ΔH=-482.6 kJ·mol-1 |
北京奥运会“祥云”火炬燃料 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2 013.8 kJ·mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 221.5 kJ·mol-1 |
A.-571.6 kJ·mol-1,-2 221.5 kJ·mol-1
B.-241.3 kJ·mol-1,-2 013.8 kJ·mol-1
C.-285.8 kJ·mol-1,-2 013.8 kJ·mol-1
D.-285.8 kJ·mol-1,-2 221.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com