
“2016年地球一小时”推出“为”蓝生活主题,鼓励公众践行可持续的生活和消费方式。下列做法与之不符的是( )
A.利用太阳能制氢
B.用家用汽车代替公交车
C.利用化石燃料制造燃料电池
D.用节能灯代替白炽灯
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年山东省济宁市高二下期末化学试卷(解析版) 题型:实验题
I. 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
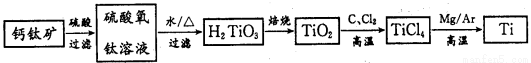
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为___________晶体。
(2)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被____个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被____个氧离子包围。

(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

化合物甲中C原子的杂化方式为_______________;化合物乙的沸点明显高于化合物甲,主要原因是_______________________________。
II. 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(4)镍元素在元素周期表中的位置为 。
(5)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(6)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(7)Ni的氯化物与氨水反应可形成配合物[Ni(NH3)4]Cl2,2mol该配合物中含有σ键______mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:选择题
化学与生活、社会、科学、技术、环境等息息相关。下列有关说法不正确的是
A. 12C和14C互为同位素,其中14C可用于文物的年代的鉴定
B.在元素周期表的金属和非金属分界线附近适合寻找半导体材料
C.“青蒿一握,以水二升渍,绞取汁”,药学家屠呦呦对青蒿素的提取属于物理变化
D.煤、石油、天然气属于重要的可再生能源,而氢氧燃料电池则是一种能量转换率较高、符合绿色化学理念的新型动力电源
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高一下期末化学试卷(解析版) 题型:选择题
下列关于乙醇的叙述中,错误的是( )
A.由于乙醇能溶解许多有机物和无机物,所以可以用乙醇提取中药中的有效成分
B.由于乙醇的密度比水小,所以混在乙醇中的水可以用分液的方法除去
C.由于乙醇能够以任意比溶解在水中,所以酒厂可以调制各种浓度的酒
D.由于乙醇易挥发,所以就有俗语“酒香不怕巷子深”的说法
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高一下期末化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.淀粉、油脂、蛋白质都能发生水解反应
B.蔗糖溶液中加入新制Cu(OH)2煮沸会析出砖红色沉淀
C.纤维素、淀粉都可用(C6H10O5)n表示,它们互为同分异构体
D.人体各种组织的蛋白质不断分解,最终生成二氧化碳和水,排出体外
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:填空题
(1)含碳物质不完全燃烧会产生剧毒的CO,根据价键理论,CO的电子式为 ,结构式为 。
(2)长期以来一直认为氟的含氧酸不存在。自1971年美国科学家用F2通过细冰末获得HFO(俗称“次氟酸”)以来,对HFO的研究引起重视。
①HFO的电子式为 ,则HFO的结构式为 (在HFO的结构式中标出各元素的化合价)。
②对比其它次卤酸可以看出,把HFO称着“次氟酸”其实不妥当的,理由是 。
③次氟酸能与水反应生成两种物质,其中有一种物质为HF(常用于雕刻玻璃),则次氟酸与水反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
下列说法错误的是
A.离子晶体在熔化状态下一定能导电
B.分子晶体的状态变化只需克服分子间作用力
C.金属键的本质是金属离子与自由电子间的相互作用
D.原子晶体中只存在非极性共价键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷(解析版) 题型:填空题
下表列出了前20号元素中的某些元素性质的一些数据:
元素 | A | B | C | D | E | F | G | H | I | J |
原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
最高 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
最低 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素中,电负性最大的是________(填元素符号)。
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:_________ _____。
②B2C2与EC2反应:____________ ____。
(3)A元素原子核外电子排布图是__ ___;比元素B原子序数大11的元素的原子的电子排布式是 ______。
(4)C和I相比较,非金属性较弱的是_____(填元素名称)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下期末化学试卷(解析版) 题型:选择题
下列与有机物结构、性质相关的叙述错误的是
A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2
B.蛋白质和油脂都属于高分子化合物,一定条件下都能水解
C.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同
D.苯 不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com