
CuCl��������ˮ�İ�ɫ���壬��һ����Ҫ�Ĵ�������ҵ�ϣ��ɿ�ȸʯ����Ҫ�ɷ�Cu(OH)2��CuCO3����FeS��FeO��SiO2���ʣ��Ʊ�CuCl��ij�������£�
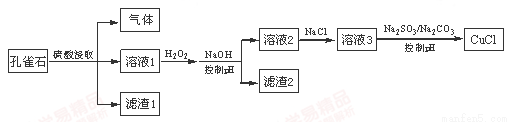
����˵������ȷ����
A��H2O2����Һ1��Fe2+����ΪFe3+����ͨ������pHת��ΪFe(OH)3��ȥ
B��SO32-����Һ3�е�Cu2+��ԭ����Ӧ�õ�CuCl
C��CO32-�����ǿ�����ҺpH����ʹCuCl����������
D�����ı��Լ�����˳����Һ3�������뵽������SO32-/CO32-����Һ�У�ͬ������ȡCuCl
 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�����У�������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�������Ȼ�ѧ����ʽ��
Zn(s)+1/2O2(g)== ZnO(s)�� ��H= ��351.1KJ/mol ,
Hg(l)+ 1/2O2(g)== HgO(s) �� ��H= ��90.7KJ/mol,�ɴ˿�֪��
Zn(s)+ HgO(s)== ZnO(s)+ Hg(l)������ͬ�����µġ�HΪ
A����441.8KJ/mol B��+260.4KJ/mol
C��+441.8KJ/mol D����260.4KJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ�����и�����ѧ�ڵڶ����ʼ컯ѧ�Ծ��������棩 ���ͣ��ƶ���
��������A�ͽ���B����ѧ��ѧ�����Ĺ��壬����A�Ե���ɫ����ͬ������A��B������Һ��C��Ӧ�ų����壬����������ǡ����ȫ��Ӧ����C������B�ڸ����µĻӷ��ԣ���ͨ������̼���κͽ�̿����ջ��������Ʊ�B��������D����Ϊ�л���Ӧ�е������Լ���1molD��1mol NH4Cl��Ӧ����2mol����E��1molB���Ȼ����֪��״��������E���ܶ�Ϊ0.76g��L-1��
��ش��������⣺
��1��E�Ļ�ѧʽΪ
��2�������Ʊ�B�Ļ�ѧ����ʽΪ ���������������̿���� ��
A.Na B.H2 C.KMnO4 D.Cl2
��3��B��E��һ�������� ������ܡ������ܡ���ֱ�ӷ�����Ӧ����D���ж������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʵ����ѧ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ�У�ֻ�ܱ�ʾһ����ѧ��Ӧ���ǣ� ��
��CO32����2H��===CO2����H2O
��Ba2����2OH����2H����SO42��===BaSO4����2H2O
��Ag����Cl��===AgCl��
��Fe��Cu2��===Fe2����Cu
��Cl2��H2O===H����Cl����HClO
A���٢� B���ڢ� C���ڢ� D��ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ���¿���������ѧ�Ծ��������棩 ���ͣ�ѡ����
�ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼת����ϵ������������ͷ�Ӧ������ȥ�������ƶϴ�����ǣ� ��
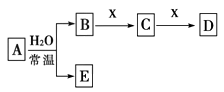
A. ��A�ĵ��ʣ�B��D�ķ�Ӧ��OH����HCO3��== H2O��CO32������E��һ��������Դ
B. ��DΪCO��C�ܺ�E��Ӧ����Aһ��ΪNa2O2�������ʽ��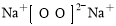
C�� ��DΪ��ɫ��������AĦ��������ȣ���Xһ��������
D����X��Na2CO3��CΪ�����Լ��ķ��ӣ���Aһ������������D��E�ܷ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʦ���и�����ѧ�ڵڶ���ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��O2��NH3�Ļ������448mLͨ�����ȵ�����������(����)����ַ�Ӧ����ͨ��������ˮ�������ռ���44��8mL������ԭ���������O2�����������(���谱ȫ������������������ѻ���ɱ�״��)( ) ��֪��NO��O2����ʱ��ˮ�ɰ�4NO+3O2+2H2O=4HNO3��Ӧ����
A��23l.5mL�� B��268.8mL C��287.5mL D��313��6mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ӦFeO��s��+C��s��= CO��g��+ Fe��s���ġ�H��0���������H����S�����¶ȱ仯���仯����������������ȷ����:
A�� ������Ϊ�Է����̣�������Ϊ���Է�����
B�� ������Ϊ�Է����̣�������Ϊ���Է�����
C�� �κ��¶���Ϊ���Է�����
D�� �κ��¶���Ϊ�Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ��Ũ�ȵ�Ũ�����м���m��ͭþ�Ͻ�ǡ����ȫ�ܽ⣨�ٶ�����Ļ�ԭ����ֻ��NO2������Ӧ��Ļ����Һ�еμ�bmol/LNaOH��Һ�����μӵ� v mLʱ��ǡ����ȫ��Ӧ���õ���������Ϊn �ˣ��������йظ�ʵ���˵������ȷ����( )
�ٳ�����������������Ϊ(n-m)�� ��ǡ���ܽ����Һ�е�NO3-���ӵ����ʵ���Ϊbv mol
�۷�Ӧ������ת�Ƶĵ�����Ϊ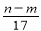 mol ������NO2��������Ϊ
mol ������NO2��������Ϊ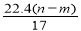 L
L
����Ͻ�Ӧ��Ӧ����������ʵ���Ϊ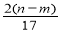 mol
mol
A���٢ڢۢܢ� B�� �٢ۢܢ� C�� �٢ۢ� D�� �٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��ء���Դ��������У������ѧ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���бȽϡ�����һ����ȷ����
A�����ԣ�HClO4>H2CO3>H2SiO3
B���ȶ��ԣ�HF<H2O<NH3
C�����Ӱ뾶��Na��>F-> Al3��
D���е㣺HI>HBr>HF
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com