
下列物质中存在配位键的是( )
①H3O+ ②[B(OH)4]- ③CH3COO- ④NH3
⑤CH4
A.①② B.①③ C.④⑤ D.②④
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.Na2O2可用于呼吸面具中氧气的来源
B.Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应,它们都是碱性氧化物
C.Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,而NaHCO3可用于治疗胃酸过多、制造发酵粉等
D.NaCl的性质稳定,可用作调味品
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质分离的叙述正确的是( )
A.用萃取分液的方法除去酒精中的水(2014·福建理综, 8C)
B.由于KNO3的溶解度大,故可用重结晶法除去KNO3中混有NaCl(2014·广东理综, 9A)
C.用分液漏斗、烧杯、蒸馏水,可完成分离Br2和CCl4混合物的实验(2014·安徽理综,9A)
D.分液时,分液漏斗中的上层液体应由上口倒出(2013·福建理综,10A)
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150 ℃和150~300 ℃的馏分。
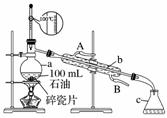
请回答下列问题:
(1)仪器a的规格和名称____________,仪器b、c的名称:b________,c________。
(2)实验所选温度计是错误的,正确的选择应该是________________________________________________________________________。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是________________________________________________________________________。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3 分子的空间构型是三角锥形,而不是正三角形的平面结构,解释该事实的充分理由是 ( )
A.NH3分子是极性分子
B.分子内3个N—H键的键长相等,键角相等
C.NH3分子内3个N—H键的键长相等,3个键角都等于107°
D.NH3分子内3个N—H键的键长相等,3个键角都等于120°
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.在分子中,两个成键的原子间的距离叫做键长
B.H—Cl的键能为431.8 kJ·mol-1,H—I的键能为298.7 kJ·mol-1,这可以说明HCl分子比HI分子稳定
C.含有极性键的分子一定是极性分子
D.键能越大,表示该分子越容易受热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列事实能说明氯元素原子得电子能力比硫元素原子强的是________(填序号)。
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大 ④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧 ⑨还原性:Cl-<S2-
(2)有三种金属元素A、B、C,在相同条件下,B的最高价氧化物的水化物的碱性比A的最高价氧化物的水化物的碱性强;若将A、C相连后投入稀硫酸中,发现C表面有明显气泡产生。则这三种金属元素的原子失电子能力由强到弱的顺序是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com