
【题目】X、Y、Z代表三种元素。已知:①![]() 和
和![]() 两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9;③Y和Z两种元素可以形成4核42电子的
两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9;③Y和Z两种元素可以形成4核42电子的![]() 价阴离子。
价阴离子。
(1)Y元素是______(填元素符号,下同),其原子的核外电子排布式为______,Z元素是______,其原子结构示意图为______
(2)由X、Y、Z三种元素形成的含68个电子的盐类化合物的化学式是______
【答案】Cl ![]() O
O 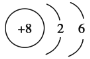
![]()
【解析】
Z元素原子核内质子数比Y元素原子核内质子数少9,可以设Z元素的核电荷数为z,则Y元素的核电荷数为z+9,Y和Z两种元素可以形成4核42电子的![]() 价阴离子,若Y和Z两种元素形成的
价阴离子,若Y和Z两种元素形成的![]() 价阴离子为Y3Z-,则3(z+9)+z=42-1,解得z=3.5,不合题意,舍去;若Y和Z两种元素形成的
价阴离子为Y3Z-,则3(z+9)+z=42-1,解得z=3.5,不合题意,舍去;若Y和Z两种元素形成的![]() 价阴离子为Y2Z2-,则2(z+9)+2z=42-1,解得z=5.75,不合题意,舍去;若Y和Z两种元素形成的-1价阴离子为YZ3-,则z+9+3z=42-1,解得z=8,则Z为O,Y为Cl。
价阴离子为Y2Z2-,则2(z+9)+2z=42-1,解得z=5.75,不合题意,舍去;若Y和Z两种元素形成的-1价阴离子为YZ3-,则z+9+3z=42-1,解得z=8,则Z为O,Y为Cl。![]() 和
和![]() 两种离子具有相同的电子层结构,所以X为K。
两种离子具有相同的电子层结构,所以X为K。
(1)根据以上分析,Y元素是Cl,其原子的核外电子排布式为![]() ,Z元素是O,其原子结构示意图为
,Z元素是O,其原子结构示意图为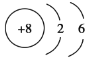 ;
;
(2)Cl形成的含氧酸盐中有1个Cl,1个K,可以计算出有4个O,所以化学式是![]() 。
。


科目:高中化学 来源: 题型:
【题目】![]() 某有机物
某有机物![]() 与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重
与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重![]() 、
、![]() ;同温同压下,
;同温同压下,![]() 蒸气的密度是
蒸气的密度是![]() 的37倍。则能够与钠反应放出
的37倍。则能够与钠反应放出![]() 的
的![]() 的结构有(不考虑立体异构)( )
的结构有(不考虑立体异构)( )
A.6种B.5种C.4种D.3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:SO2(g)+1/2O2(g)![]() SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )
SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )
A. 3/2B. 2/3C. 6/5D. 5/6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中正确的是
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③除去溴苯中的少量溴:加入NaOH溶液,振荡、静置分层后,除去水层
④除去乙酸乙酯中残留的乙酸,加过量饱和![]() 溶液振荡后,静置分液
溶液振荡后,静置分液
⑤塑料、橡胶和光导纤维都是合成高分子材料
⑥石油的分馏、裂化和煤的干馏都是化学变化
A.①⑤⑥B.①②③⑤C.②③④D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽油不仅是最重要的燃料,而且是重要的化工原料,它既可以裂解得到气态化工原料如乙烯等,还可以在催化剂催化下改变分子结构,由链烃变成芳香烃,如己烷变成苯,庚烷变成甲苯等。又知丙烯的化学性质和乙烯相似,请根据如图,回答有关问题:
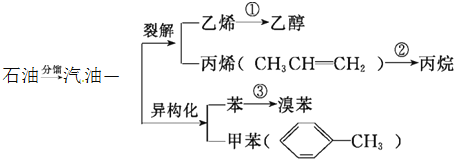
(1)写出相应的化学方程式:
![]() ______;
______;
![]() ______;
______;
![]() ______;
______;
(2)甲苯分子里苯环上一个氢原子被硝基取代后的产物有 ______ 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将纯净的SO2气体通入0.1molL﹣1的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2;
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.
实验步骤 | 实验现象 | 结论 |
实验1:在盛有不含O2的25mL0.1molL﹣1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | _______ | 假设一成立 |
实验2:在盛有不含O2的25mL0.1molL﹣1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | ________ |
为深入研究该反应,该小组还测得上述两个实验中溶液pH随通入SO2体积的变化曲线如图。实验1中溶液pH变小的原因是____________;V1时,实验2中溶液pH小于实验1的原因是__________。(用离子方程式表示)
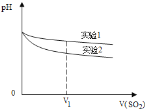
(2)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论:
实验步骤 | 实验现象 | 结论 |
__________________ | ______________ | 假设二成立 |
(3)若假设二成立,请预测:在相同条件下,分别用足量的O2和KNO3氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反应后两溶液的pH前者_____________(填“大于”或“小于”)后者,理由是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池结构示意图如下。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。下列说法正确的是( )
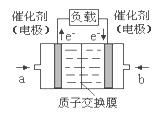
A.电解质溶液中,H+向左移动
B.负极反应式为:CH3OH+H2O-6e-=CO2+6H+
C.b处通入甲醇,a处通入空气
D.正极反应式为:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H2SO4、HNO3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图:

(1)还原过程中主要反应的离子方程式为_______。
(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称__________,有关抽滤,下列说法正确的是__________
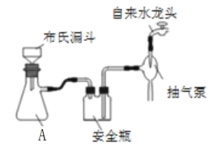
A.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶上口倒出
B.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸
D.减压过滤不宜用于过滤胶状或颗粒太小的沉淀
(3)操作1为马上再洗涤,然后在真空干燥机内于70℃干燥2h,冷却、密封包装。其中最合理的洗涤试剂__________
A. 浓盐酸 B. 浓氨水 C. 无水乙醇 D. 水+乙醇
真空干燥的原因是___________。
(4)随着pH减小,Cu2(OH)4-nCln中铜的质量分数__________
A. 增大 B. 不变 C. 减小 D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲元素原子的![]() 能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
(1)甲的元素符号是______;其电子排布图为______。
(2)乙元素原子的最外层电子排布式为______,其在元素周期表中的位置是______。
(3)甲属于______区元素,乙属于______区元素。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com