


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、硫酸钠溶液与氯化钡溶液 |
| B、铝片与硝酸汞溶液 |
| C、稀硫酸与铜片 |
| D、硝酸钠溶液与氯化钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中性溶液就是PH=7的溶液 |
| B、中性溶液是指c(H+)=c(OH-)的溶液 |
| C、酸与碱恰好完全中和所得的溶液是中性溶液 |
| D、不能使酸碱指示剂显色的溶液是中性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

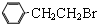 通过消去反应制备Ⅰ的化学方程式为
通过消去反应制备Ⅰ的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:

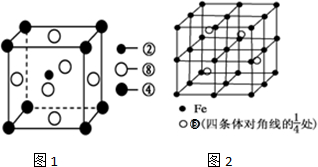
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素.A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,其氢化物能和一种半导体材料反应生成常温常压下的两种气体;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍.请回答下列问题:
A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素.A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,其氢化物能和一种半导体材料反应生成常温常压下的两种气体;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室用乙醇与浓硫酸共热制取乙烯,常因温度过高生成少量SO2,有人设计了如图所示实验,以验证上述混合气体中是否含有乙烯和SO2.
实验室用乙醇与浓硫酸共热制取乙烯,常因温度过高生成少量SO2,有人设计了如图所示实验,以验证上述混合气体中是否含有乙烯和SO2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com