
自发进行的反应一定是( )
A.吸热反应 B.放热反应
C.熵增加反应 D.熵增加或者放热反应
科目:高中化学 来源: 题型:
已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是________溶液
(2)各取5mL上述溶液,分别加热(温度相同),pH较小的是________溶液
(3)H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)之比为__________
(4)取5mL NH4Cl溶液,加水稀释至50mL,c(H+) ____________ 10-6mol·L-1(填“>”、“<”或“=”),c(NH4+)/c(H+)_______________(填“增大”、“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
S-诱抗素制剂能保持鲜花盛开,S-诱抗素的分子结构
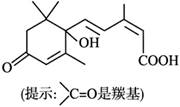 如图,下列关于该物质说法正确的是
如图,下列关于该物质说法正确的是
A. S-诱抗素制剂能发生酯化反应的官能团有2种
B. 含有苯环、羟基、羰基、羧基、碳碳双键
C. 1 mol S-诱抗素制剂与足量金属Na反应生成0.5 mol H2
D. 该化合物不能发生聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(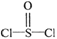 )中而形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响。
B.金属锂作电池的正极,石墨作电池的负极。
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3。
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:l。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验证明,多数能自发进行的反应都是放热反应。对此说法的理解正确的是( )
A.所有的放热反应都是自发进行的
B.所有的自发反应都是放热的
C.焓变是影响反应是否具有自发性的一个重要因素
D.焓变是决定反应是否具有自发性的唯一判据
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用赤铁矿生产铁,可以选择的还原剂有C和H2。根据所学的知识判断:哪一种还原剂可使反应自发进行的温度较低?
已知:Fe2O3(s)+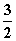 C(s)===2Fe(s)+
C(s)===2Fe(s)+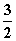 CO2(g)
CO2(g)
ΔH=233.8 kJ·mol-1,ΔS=0.279 kJ·mol-1·K-1
Fe2O3(s)+3H2(g)===2Fe(s)+3H2O(g)
ΔH=98 kJ·mol-1,ΔS=0.144 2 kJ·mol-1·K-1
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用浓盐酸分别与KMnO4、MnO2、KClO3等多种物质在一定条件下反应制取氯气
①上述反应中,HCl表现的性质是________、________。
②在常温下,浓盐酸与KMnO4可反应生成氯气,KMnO4中的Mn被还原为+2价,该反应的化学方程式:__________________________________________________________________
________________________________________________________________________。
③KMnO4、MnO2和Cl2的氧化性由强到弱的顺序是:
________________________________________________________________________。
④已知KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O,用双线桥表示该反应的电子转移情况:
________________________________________________________________________。
⑤用上述三种物质分别制取标准状况下3.36 L氯气时,转移的电子数分别是__________________(NA表示阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A(C8H17Br)经NaOH醇溶液处理后生成两种烯烃B1和B2。B2(C8H16)经过:①用臭氧处理;②在Zn存在下水解,只生成一种化合物C。C经催化氢化吸收1 mol氢气生成醇D(C4H10O),用浓硫酸处理D只生成一种无侧链的烯烃E(C4H8)。已知:(注:R1、R3可为H或其他烃基)

试根据已知信息写出下列物质的结构简式:
A________;B2________;C________;E________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com