
【题目】对于aA(g)+bB(g)cC(g)反应,改变某一变量(条件)得到如图象(p 表示压强,T 表示温度,n 表示物质的量,á 表示平衡转化率).根据图象,下列判断正确的是( )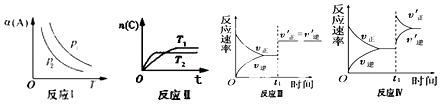
A.反应 I:若 p1>p2 , 则 a+b<c
B.反应Ⅱ:此反应的△H<0,且 T1<T2
C.反应Ⅲ:表示t1 时刻一定是使用催化剂对反应速率的影响
D.反应Ⅳ:表示t1时刻增大 B 的浓度对反应速率的影响
【答案】B
【解析】解:A.若 p1>p2,可知压强越大,A的转化率越大,则增大压强,平衡正向移动,则a+b>c,故A不符合题意;
B.由图可知T1<T2,温度高时C的物质的量小,可知升高温度平衡逆向移动,则此反应的△H<0,故B符合题意;
C.若a+b=c,增大压强时正逆反应速率同等程度增大,则催化剂、加压均符合图中速率变化,故C不符合题意;
D.增大 B 的浓度,瞬间逆反应速率不变,与图中逆反应速率瞬间增大不符,故D不符合题意;
故选B.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
【题目】(1)某有机物由C、H、O三种元素组成,球棍模型如图所示:

①含有的官能团名称是_______;
②写出此有机物与金属钠反应的化学方程式_______。
(2)四种常见有机物分子的比例模型示意图如下,其中甲、乙、丙为烃,丁为烃的衍生物。

①可以鉴别甲和乙的试剂为_________;
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
②上述物质中有毒、有特殊气味,且不溶于水、密度比水小的是_________(填名称),将其加入溴水中,振荡后静置,观察到的现象是_______。
③乙和丁的物质的量共1.5mol,完全燃烧需要的氧气的物质的量是_______。
(3)乳酸(![]() )是一种有机物,它在多种生物化学过程中起重要作用。
)是一种有机物,它在多种生物化学过程中起重要作用。
①1mol乳酸与足量的Na反应生成氢气的物质的量是_______。
②乳酸与铁粉反应生成乳酸亚铁,可用于治疗缺铁性贫血。反应的化学方程式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以对甲苯酚A为起始原料,通过一系列反应合成有机物G和F。

已知:

 (羟醛缩合反应)
(羟醛缩合反应)
(1)D中含氧的官能团______________ ⑥反应类型_______________。
(2)若C和甲乙酮(![]() )在上述条件下,发生类似Ⅱ的反应产生互为同分异构体的两种有机物,写出它们的结构简式______________________________、_______________________________。
)在上述条件下,发生类似Ⅱ的反应产生互为同分异构体的两种有机物,写出它们的结构简式______________________________、_______________________________。
(3)写出反应②的化学方程式____________________________________________________________。
(4)在反应⑤之前增加步骤④的目的是___________________________。
(5)符合下列条件的F同分异构体有__________种
①发生银镜反应 ②与FeCl3溶液发生显色反应 ③苯环上一氯代物有两种
(6)参照上述合成路线和相关信息,设计以乙醛为原料(无机试剂任选)制备高级吸水性树脂 的合成路线_____________。
的合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲测定市场上某H2O2消毒液质量分数,现进行如下操作
己知:2MnO4﹣+5H2O2+6H+═2Mn2++8H2O+5O2
操作①:取10.00mLH2O2溶液(密度为1.00gmL﹣1)置于锥形瓶中加水稀释,再加稀硫酸酸化;
操作②:用0.200 0molL﹣1KMnO4溶液滴定;
操作③:用同样方法滴定,4次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00mL.请回答下列问题:
(1)滴定时盛装KMnO4溶液应选取的仪器是(填序号).
A.50mL酸式滴定管
B.50mL碱式滴定管
C.25mL酸式滴定管
D.25mL碱式滴定管
(2)是否需要选用指示剂(填“是”或“否”)达到滴定终点的现象是 .
(3)分析数据,计算该H2O2溶液中溶质的质量分数为(保留三位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:

(1)两种方法的沉淀池中均发生的反应化学方程式为______________________________。
(2)X是_________,Y是__________(填化学式)。
(3)Z中除了溶解的氨气、食盐外,其它溶质还有____________________;排出液中的溶质除了氢氧化钙外,还有______________________________________________。
(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是_______。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
(5)为检验产品碳酸钠中是否含有氯化钠,请设计实验方案__________________________。
(6)联碱法中,每当通入NH3 22.4L(已折合成标准状况下)时可以得到纯碱50.0g,则NH3的利用率为____________。(结果精确到0.01)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶性离子是大气颗粒物的主要成分,研究其化学组成对于治理大气污染其有重大意义,某地区大气颗粒物经采样与必要的预处理后得试样溶液。经离子色谱检验确定含有以下离子NH4+、Na+、Mg2+、Ca2+、Al3+、SO42-、NO3-、CO32-、Cl-。某同学对其再进行如下的实验:
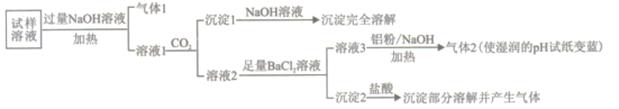
已知:在加热与强碱性条件下,铝单质可以将NO3-还原为氨气。
回答下列问题:
(1)“气体1“的电子式为_________。
(2)生成“沉淀1”的离子方程式为________。
(3)“沉定2”的成分是___________(填化学式)。
(4)“溶液3![]() 气体2”的离子方程式为_________。
气体2”的离子方程式为_________。
(5)根据上述实验可推断该地区大气颗粒物中__________含量较低(填离子符号)。
(6)已知大气颗粒物中各元素的行染主体如下表:
元素 | N | S | Na、Mg、Cl | Al | Ca |
污染主体 | 机动车尾气 | 燃煤污染 | 海盐离子 | 土壤扬尘 | 建筑粉尘 |
根据实验结果可判断该地区大气颗粒物污染主体有___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
A.加热
B.不用稀硫酸改用98%的浓硫酸
C.滴加少量硫酸铜溶液
D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2CO3和H2SO3的电离常数如下表:
酸 | Ka1 | Ka2 |
H2CO3 | 4.27×10-7 | 5.61×10-11 |
H2SO3 | 1.54×10-2 | 1.02×10-7 |
向10mL0.1mol/LNa2CO3溶液中滴加0.1mol/LH2SO3溶液,测得溶液pH随加入H2SO3溶液体积的变化如图所示。
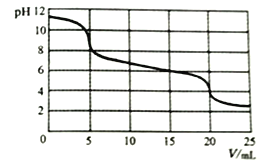
下列说法不正确的是
A. 加入H2SO3溶液前,Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
B. 0<V<5时,溶液中反应为:H2SO3+CO32-==HCO3-+HSO3-
C. 15<V<20时,溶液中反应为:H2SO3+HCO3-==HSO3-+CO2↑+H2O
D. V=15时,所得溶液中:(HCO3-)<c(HSO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二氧化碳和氢气在一定条件下可以合成甲醇,其制备反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下列说法正确的是
CH3OH(g)+H2O(g),下列说法正确的是
A. 调控反应条件不能改变反应限度
B. 化学反应的限度决定了反应物在该条件下的最大转化率
C. 当CO2的消耗速率等于其生成速率时,该反应已停止
D. 投入1molCO2能得到1mol的CH3OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com