
体积相同的甲.乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2⇌2SO3,并达到平衡.在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率()
A . 等于p% B. 大于p% C. 小于p% D. 无法判断
. 等于p% B. 大于p% C. 小于p% D. 无法判断
考点: 化学平衡的计算.
专题: 化学平衡专题.
分析: 先假定甲、乙的体积都不变,达到平衡后再保持乙的压强不变,此反应是气体体积减小的反应,因此,待等体积达平衡后,欲保持乙的压强不变,就需要缩小体积.缩小体积则乙的压强增大,平衡正向移动.
解答: 解:先假定甲、乙的体积都不变,达到平衡后再保持乙的压强不变,此反应是气体体积减小的反应,因此,待等体积达平衡后,欲保持乙的压强不变,就需要缩小体积.缩小体积时,乙的压强增大,平衡正向移动.所以,若甲容器中SO2的转化率为P%,则乙的SO2的转化率将大于甲的,即大于P%.
故选B.
点评: 这一类问题的解决方法一般如此,先设为同等条件,平衡后再改变某一条件使之符合题设条件,分析变化.这样,问题就迎刃可解了.


科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)═2HCl(g)的反应热(△H)等于﹣183kJ/mol,又知H﹣H键的键能为436kJ/mol,Cl﹣Cl键的键能为243kJ/mol,则H﹣Cl键的键能为()
A. 248kJ/mol B. 496kJ/mol C. 862kJ/mol D. 431kJ /mol
/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式C2H2(g)+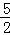 O2(g)═2CO2(g)+H2O(g)△H=﹣1256kJ/mol,下列说法正确的是()
O2(g)═2CO2(g)+H2O(g)△H=﹣1256kJ/mol,下列说法正确的是()
A. 乙炔(C2H2)的燃烧热为1256 kJ/mol
B. 若转移10 mol电子,则消耗2.5 mol O2
C. 若生成2 mol液态水,则△H=﹣2512 kJ/mol
D. 若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是()
A. ①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上可利用合成气(CO和H2的混合气体)生产甲醇.已知:CO(g)+2H2(g)⇌CH3OH(g)△H=﹣92.9kJ/mol一定条件下,该反应在一体积固定的密闭容器中达到平衡.下列说法正确的是()
A. 该反应的△S<0
B. 该反应在任何温度下均能自发进行
C. 向容器中充入少量He,平衡向正反应方向移动
D. 升高温度平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,摩托罗拉公司开始了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.如图是一个电化学过程的示意图.已知甲池总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O
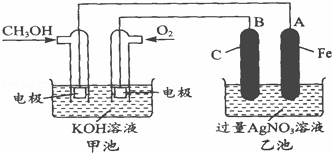
请填空:
(1)充电时:①原电池的负极与电源负极相连.②阳极的电极反应式为
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质增加648g,则甲池中理论上消耗O2 L(标准状况下).
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是()
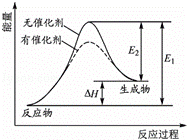
A. 该反应为吸热反应
B. 催化剂能改变反应的焓变
C. 催化剂能降低反应的活化能
D. 逆反应的活化能大于正反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1273K时发生反应Fe(s)+H2O(g)⇌FeO(s)+H2(g);现在固定容积为2.0L的密闭容器中进行该反应,试解答下列问题:
(1)其他条件不变,缩小该容器体积,反应速率增 (填“增大”、“减小”或“不变”)
(2)若降温后H2的百分含量减少,则正反应是 反应(选填“吸热”、“放热”).
(3)能判断该反应达到化学平衡状态的依据是 ;
a.混合气体的压强保持不变
b.H2的浓度不再改变
c.消耗H2O的物质的量与生成H2的物质的量之比为1:1
d.Fe、H2O、FeO、H2的物质的量之比为1:1:1:1.
查看答案和解析>>
科目:高中化学 来源: 题型:
C、N、S都是重要的非金属元素.下列说法正确的是()
A. 三者对应的氧化物均为酸性氧化物
B. 三者的单质直接与氧气反应都能至少生成两种氧化物
C. 相同温度下,等物质的量浓度的Na 2CO3、NaNO3、Na2SO3溶液的pH大小顺序:NaNO3<Na2S03<Na2CO3
2CO3、NaNO3、Na2SO3溶液的pH大小顺序:NaNO3<Na2S03<Na2CO3
D. CO2、NO2、SO2都能与H2O反应,其反应原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com