

| ������ | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ����pH | 2.7 | 7.6 | 4.7 |
| ��ɳ���pH | 3.2 | 9.7 | 6.7 |
���� ��ȡ������CuCl2•2H2O�������̿�֪������aΪ�������������������ӣ����������������ʣ���aΪH2O2��Һ������pH��3.2��pH��4.4ʹ������ת��Ϊ������Ȼ����ˣ���Һ��HCl�����������ᾧ�õ�CuCl2•2H2O���Դ������
��� �⣺��ȡ������CuCl2•2H2O�������̿�֪������aΪ�������������������ӣ����������������ʣ���aΪH2O2��Һ������pH��3.2��pH��4.4ʹ������ת��Ϊ������Ȼ����ˣ���Һ��HCl�����������ᾧ�õ�CuCl2•2H2O��
��1�������м�����Լ�a����ʵ���C����Ŀ���ǽ�Fe2+�������ʴ�Ϊ��C����Fe2+������
��2������ͭ��������ͭ���ɴٽ�������ˮ��ת��Ϊ�������Ȼ�ͭ���ܣ���NaOH����߾���Ӧ���ܳ��ӣ��ʴ�Ϊ��AC��
��3������ȴٽ�ͭ����ˮ�⣬���ɵ�HCl�ӷ�������ֱ�������ᾧ�õ�CuCl2•2H2O���ʴ�Ϊ�����ܣ�
���� ���⿼����������ᴿ���ۺ�Ӧ�ã�Ϊ��Ƶ���㣬���������еķ�Ӧ���������뷽����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע������ˮ�⡢������ԭ��Ӧ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | C2H4 | C�� | ����ϩ | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
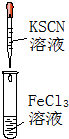 | 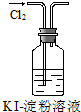 | 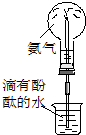 | 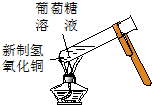 |
| �� | �� | �� | �� |
| A�� | ʵ����Թ��л����Һ�г��ֺ�ɫ���� | |
| B�� | ʵ�������Һ���ɫ | |
| C�� | ʵ�������ƿ����Һ���ɫ | |
| D�� | ʵ����г��ֺ�ɫ����ͭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| װ�� | ���� | ���ۼ����� |
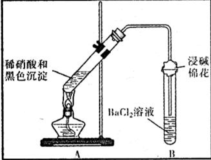 | ��A�Թ��к�ɫ�������ܽ� ��A�Թ��Ϸ����ֺ���ɫ���� ��B�Թ��г��ְ�ɫ���� | a�������˵����ɫ�������� ��ԭ�ԣ� b���Թ�B�в�����ɫ�������ܷ�Ӧ�����ӷ���ʽΪ NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɷǵ��������ˮ�õ�����Һ | |
| B�� | [H+]��[OH-]��Ϊ5.0��10-7mol•L-1����Һ | |
| C�� | �����ʵ�����ǿ����ǿ�Ӧ�õ�����Һ | |
| D�� | ��pH=9���ռ���Һϡ��100�����õ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��˵��H2CO3��������ʣ�HCO3-+H2O?H2CO3+OH- | |
| B�� | ��˵���ܽ���AgClǿ��AgI��AgCl+I-�TCl-+AgI | |
| C�� | ��˵��������ǿ�HCl+AgNO3�TAgCl��+HNO3 | |
| D�� | ��˵��NH3���H+������H2Oǿ��NH3+H3O+�TNH4++H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
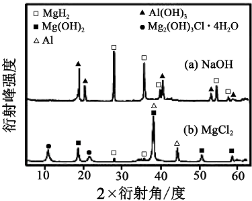
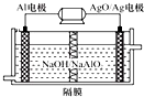
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �õ�طŵ�ʱ�������ĵ缫��ӦΪO2+4H++4e-�T2H2O | |
| B�� | �õ�س��ʱ������������������Ӧ��Li++e-�TLi | |
| C�� | ����е��л����Һ������ϡ������� | |
| D�� | ������������LiOH�ɻ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
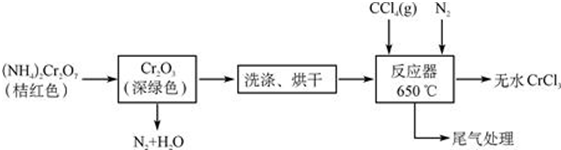
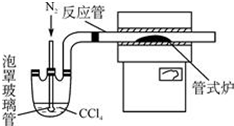
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com