
| A. | 放电时,电解质溶液中K+移向负极 | |
| B. | 放电时,电解质溶液的pH 不变 | |
| C. | 充电时,阴极的反应为:Zn(OH)42-+2e-=Zn+4OH- | |
| D. | 充电时,当有4.48L 氧气(标准状况下)释放出来时,则析出固体Zn为13g |
分析 根据2Zn+O2+4OH-+2H2O═2Zn(OH)42-可知,O2中元素的化合价降低,被还原,应为原电池正极,电极反应为:O2+4e-+2H2O=4OH-,Zn元素化合价升高,被氧化,应为原电池负极,电极反应为:Zn-2e-+4OH-=Zn(OH)42-,放电时阳离子向正极移动,充电与放电过程相反,以此解答该题.
解答 解:A.放电时,为原电池,溶液中阳离子向正极移动,即K+向正极移动,故A错误;
B.放电时,消耗氢氧根,碱性减弱,PH值减小,故B错误;
C.充电时,阳极上发生失电子的氧化反应,阴极上发生得电子的氧化反应,则阴极反应为:Zn(OH)42-+2e-=Zn+4OH-,故C正确;
D.产生1mol氧气,转移电子为4mol,充电时,当有4.48L 氧气(标准状况下)释放出来时,转移电子物质的量为:$\frac{4.48L}{22.4L/mol}$×4=0.8mol,根据Zn~2e-,则析出固体Zn为:$\frac{0.8mol}{2}$×65g/mol=26g,故D错误;
故选C.
点评 本题考查原电池与电解池的基础知识,正确判断正负极、阴阳极,注意电极反应式的书写及电子转移的计算,正确判断化合价的变化为解答该题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | MgO熔点高 | 可用作耐火材料 |
| B | KMnO4具有强氧化性 | 可用于漂白织物 |
| C | 常温下,铁能被浓硫酸钝化 | 常温下,可用铁质器皿盛放浓硫酸 |
| D | TiCl4在水中能发生水解 | 可用TiCl4溶液制备TiO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 物质 | 杂质 | 试剂或用品 | 主要操作 | |
| A | 淀粉 | 碘化钾 | 半透膜 | 渗析 |
| B | Fe(NO3)2 | Ba(NO3)2 | 硫酸 | 过滤 |
| C | Fe | I2 | / | 加热 |
| D | 溴 | 四氧化碳 | 蒸馏装置 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
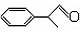 )曾入选伦敦奥运会指定产品,下面是工业合成龙葵醛的路线图(部分反应条件及副产物已略去),回答问题:
)曾入选伦敦奥运会指定产品,下面是工业合成龙葵醛的路线图(部分反应条件及副产物已略去),回答问题: $→_{催化剂}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化剂}$龙葵醛
$→_{催化剂}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化剂}$龙葵醛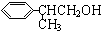 +O2
+O2
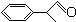 +2H2O.
+2H2O. 或
或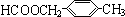 (任写一种).
(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
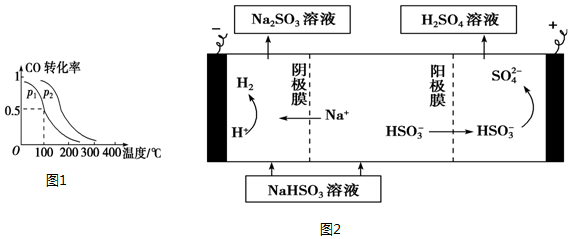
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0gH218O与D216O的混合物中所含中子数为NA | |
| B. | 0.1molCl2溶于足量水中,转移的电子数为0.1NA | |
| C. | 常温常压下50g 46%的乙醇溶液中,所含氧原子数目为0.5NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活污水使用明矾杀菌消毒 | B. | 向燃煤中加入适量石灰石“固硫” | ||
| C. | 推广使用可降解塑料防止白色污染 | D. | 提倡公交出行可减少氮氧化物排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | 活性炭可吸附水中的悬浮物 | 用于自来水的杀菌消毒 |
| B | SO2具有还原性 | 漂白纸浆 |
| C | 铁被氧气氧化时会放出热量 | 铁、活性炭、无机盐、水等的混合物制成暖宝贴 |
| D | 氧化铝是两性氧化物 | 作耐高温材料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com