
某学生做如下实验:第一步,在淀粉?KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列对实验原理的解释和所得结论错误的是( )
A. 蓝色逐渐消失的原因是Na2SO3溶液具有漂白性
B. 第一步反应的离子方程式ClO-+2I-+2H+===I2+Cl-+H2O
C. 淀粉?KI溶液变蓝是因为I-被氧化为I2,I2使淀粉变蓝色
D. 微粒的氧化性由强到弱的顺序是ClO->I2>SO
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2016-2017学年湖南长沙市新高一分班考试化学(解析版) 题型:填空题
周末回家,妈妈为小昊准备的午餐有:米饭、鱼、肉、小白菜和豆腐汤,这些食物中含有的营养物质有蛋白质、 、 、维生素、油脂、水和无机盐。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第一次月考(开学考试)化学(解析版) 题型:实验题
(10分)常温下,现有A、B、C、D四种电解质分别完全溶于水,所得四种溶液中含H+、Ba2+、Al3+、Na+、HCO3-、Cl-、OH-、SO42-八种离子(不考虑水解)。为了检验这四种物质,进行如下实验:
①取少量A的溶液分别与另三种物质反应,依次观察到:白色沉淀和气体、气体、白色沉淀。
②经测定,A和D的溶液显碱性,B和C的溶液pH<7。B与D的溶液反应产生两种沉淀,当D的量增大时,其中一种沉淀不断溶解,最终还存在一种沉淀。
③C与D的溶液反应,无明显现象。经测定,该反应的产物总能量小于反应物总能量。
根据上述实验事实,请回答下列问题:
(1)C的名称是________,D的化学式_________。
(2)用离子方程式表示A的溶液显碱性的原因:_________________。
(3)A与B在溶液中反应的离子方程式为________________。
(4)等物质的量浓度、等体积的B和D的溶液混合,写出反应的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第一次月考(开学考试)化学(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有( )
①0.2mol H2O2完全分解转移的电子数为0.4NA
②25℃、101kPa下,16gO3和O2混合气体中含有的氧原子数为NA
③将含0.1molFeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1molFe溶于过量稀硝酸,电子转移数为3NA
⑤标准状况下,22.4LCHCl3中含有的氯原子的数目为3 NA
A.①②③ B.①②④⑤ C.①②③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:实验题
(10分)
(1)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3) ②NaHCO3(Na2CO3)
③Cl2 (HCl) ④SiO2 (Fe2O3)
(2)将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(容器不参与反应)。试判断下列情况下,溶液中存在的金属离子和金属单质。
①若铁粉有剩余,则容器中不可能有的离子是________________;铜单质________(填“一定”或“可能”)存在。
②若氯化铜有剩余,则容器中还可能有的离子为________;铜单质__________(填“一定”或“可能”)存在。
③若氯化铁和氯化铜都有剩余,则容器中不可能有的单质是______,Fe2+_______(填“一定”或“可能”)存在。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
绿泥石的组成可表示为Al4Si4Ox(OH)y,其中x、y分别为( )
A.10 8 B.7 10 C.8 10 D.9 7
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
化学在生活中有着广泛的应用,下列对应关系错误的是( )
化学性质 | 实际应用 | |
A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南衡阳八中高三实验班暑期第一次月考理综化学(解析版) 题型:选择题
根据如图的转化关系判断下列说法正确的是(反应条件已略去)
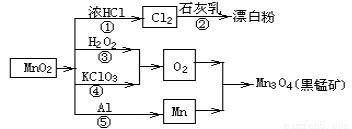
A.反应①②③④⑤均属于氧化反应和离子反应
B.反应⑤说明该条件下铝的还原性强于锰
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1
D.反应①中氧化剂与还原剂的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源:2017届河北沧州市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:

下列说法不正确的是
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中△H1=△H2+△H3 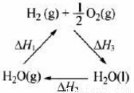
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH――2e-═CO32-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com