
【题目】Ⅰ.现有下列八种物质: ①铝 ②蔗糖 ③SiO2 ④H2SO4 ⑤NaOH ⑥FeSO4溶液 ⑦Ba(OH)2 ⑧氢氧化铁胶体。
(1)上述物质属于电解质的有____________(填序号,下同),能导电的有__________。
(2)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH===H2O,则该反应的化学方程式为____________。
(3)实验室制备⑧的离子方程式为__________________。若在⑧中缓慢加入④的溶液,产生的现象是________________________。
(4)③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为_______________。工艺师常用_______(填物质名称)来雕刻玻璃。
Ⅱ.下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(1)分离CCl4和H2O:___________。
(2)除去澄清石灰水中悬浮的CaCO3: ___________。
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:__________。
【答案】④⑤⑦ ①⑥⑧ H2SO4+2NaOH===Na2SO4+2H2O Fe3++3H2O![]() Fe(OH)3(胶体)+3H+ 随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液 SiO2+2NaOH===Na2SiO3+H2O 氢氟酸 A B D
Fe(OH)3(胶体)+3H+ 随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液 SiO2+2NaOH===Na2SiO3+H2O 氢氟酸 A B D
【解析】
Ⅰ.(1)电解质是在水溶液中或熔融状态下能导电的化合物。
(2)能发生H++OH=H2O的离子反应,则满足条件是强酸强碱生成可溶性盐和水的反应。
(3)实验室制备氢氧化铁胶体的离子方程式为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+。
Fe(OH)3(胶体)+3H+。
(4)二氧化硅与氢氧化钠溶液反应的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O,因4HF+SiO2=SiF4↑+2H2O,工艺师常用氢氟酸来雕刻玻璃。
Ⅱ.(1)CCl4和H2O互不相溶,可用分液法分离。 (2)除去澄清石灰水中悬浮的CaCO3可用过滤法分离。(3)CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)沸点相差较大,可用蒸馏法分离。
Ⅰ.(1)电解质是在水溶液中或熔融状态下能导电的化合物,则上述物质属于电解质的有④⑤⑦,其中能导电的有①⑥⑧(氢氧化铁胶粒带电),故答案为:④⑤⑦;①⑥⑧。
(2)能发生H++OH=H2O的离子反应,则满足条件是强酸强碱生成可溶性盐和水的反应,符合此条件的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O,故答案为:H2SO4+2NaOH=Na2SO4+2H2O。
(3)实验室制备氢氧化铁胶体的离子方程式为: Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,若在此胶体中缓慢加入稀硫酸,随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液,故答案为:Fe3++3H2O
Fe(OH)3(胶体)+3H+,若在此胶体中缓慢加入稀硫酸,随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液,故答案为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+;随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液 。
Fe(OH)3(胶体)+3H+;随着H2SO4溶液的逐渐加入先产生红褐色沉淀,后沉淀逐渐溶解最后得到棕黄色溶液 。
(4)二氧化硅与氢氧化钠溶液反应的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O,4HF+SiO2=SiF4↑+2H2O,工艺师常用氢氟酸来雕刻玻璃,故答案为:SiO2+2NaOH=Na2SiO3+H2O;氢氟酸。
Ⅱ.(1)CCl4和H2O互不相溶,可用分液法分离,故选A;
(2)除去澄清石灰水中悬浮的CaCO3可用过滤法分离,故选B;
(3)CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)沸点相差较大,可用蒸馏法分离,故选D。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】碱式碳酸铜可用于有机催化剂、杀虫剂及饲料中铜的添加剂,还可用于烟火和颜料制造。CuSO4溶液与Na2CO3溶液反应能否得到碱式碳酸铜?某班同学进行相关探究。
(沉淀制备)取一定量胆矾(CuSO4·5H2O)溶于水,再滴几滴稀硫酸,充分搅拌后得到一定体积的CuSO4溶液。向其中加适量Na2CO3溶液,将所得蓝绿色悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。
(1)用无水乙醇洗涤的目的是________。
(实验探究)同学们设计了如下装置,用制得的蓝绿色固体进行实验:
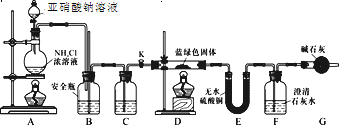
(2)D装置加热前,需要首先打开活塞K,用A装置制取适量N2,然后关闭K,点燃D处酒精灯。A中产生的N2将装置中的空气排除,避免干扰。C中盛装的试剂应是________。
(3)装置A中发生反应的离子方程式为________。
(4)若蓝绿色固体的组成为xCuCO3·yCu(OH)2,实验能观察到的现象是________。
(5)同学们查阅文献知:Ksp(CaCO3)=2.8×10-9,Ksp(BaCO3)=5.1×10-9,经讨论认为需要用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式,其原因是________。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
(6)待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是________。若定量分析所取蓝绿色固体质量为27.1 g,装置F中使用Ba(OH)2溶液,实验结束后,装置E的质量增加2.7 g,F中产生沉淀19.7 g。则该蓝绿色固体的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,能长时间保持稳定的放电电压。其电池总反应为:3Zn + 2K2FeO4 + 8H2O![]() 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-= Zn(OH)2
B. 充电时阳极发生氧化反应,附近溶液碱性增强
C. 充电时每转移3mol电子,阴极有1.5molZn生成
D. 放电时正极反应为:FeO42- + 3e- + 4H2O = Fe(OH)3 + 5OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下2 mL 1 mol·L-1 NaHCO3溶液,pH约为8,向其中滴加几滴饱和CaCl2溶液,有白色沉淀和无色气体生成。下列说法中,不正确的是
A. NaHCO3溶液中,HCO3-水解程度大于其电离程度
B. NaHCO3溶液中,c(Na+) > c(HCO3-) > c(OH-) > c(H+)
C. 最终所得的混合溶液中,c(Na+) + c(H+) = c(HCO3-) + 2c(CO32-)+ c(OH-)
D. 滴加饱和CaCl2溶液促进了HCO3-的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HA 为一元弱酸。已知溶液中HA、A-的物质的量分数δ随溶液pH变化的曲线如图所示。向10 mL0.1mol/LHA溶液中,滴加0.1mol/LNaOH溶液x mL。下列说法中,不正确的是

A. pH=9时,c(A-)=c(HA)
B. x=0时,1
C. HA的电离平衡常数ka=10-5
D. x=10时,c(A-)+c(HA)=c(Na+)=0.05mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关,下列说法正确的是
A. 涤纶、有机玻璃、光导纤维都是有机高分子化合物
B. 大豆中含有丰富的蛋白质,豆浆煮沸后蛋白质变为了氨基酸
C. 棉花和合成纤维的主要成分均为纤维素
D. 常用于制备染料、医药、农药等的酚类物质可来源于煤的干馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4v正(O2)=5v逆(NO)
B. 若单位时间内生成xmol NO的同时,消耗xmolNH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率的关系是2v正(NH3)=3v正(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com